3-甲基戊二酸尿症1型(3-MGA-I)患儿性早熟
来源:医博士 | 2021-05-12 作者:刘雅丽
3-甲基戊二酸尿症1型(3-MGA-I)(MIM ID#250950)是一种非常罕见的常染色体隐性有机酸尿症。3-MGA-I来自突变的AUH基因,编码3-甲基戊二酸辅酶a水合酶(3-MGH)。3-MGH催化亮氨酸降解的一个步骤,即3-甲基戊二酸-CoA转化为3-羟基-3-甲基戊二酸-CoA。
因此,尿中3-甲基戊二酸(3-MGA)的排泄量显著增加,3-甲基戊二酸(3-MG)和3-羟基异戊酸(3-HIVA)轻度增加是3-MGA-I的特征,可通过尿有机酸分析进行测量。
3-MGA-1的临床特征具有异质性。在儿童时期,可以从无症状个体到轻度神经损伤、言语延迟、四肢瘫痪、肌张力障碍、舞蹈样运动、严重脑病、精神运动障碍、基底节受累等临床表现。在成人发病的情况下,报道过缓慢进行性白质脑病伴有进行性痴呆、共济失调和痉挛。
早期的饮食治疗如限制亮氨酸和补充肉碱可能有效改善3-MGA-1患儿的神经状态。因此,3-MGA-1被包括在一些新生儿筛查检测(NBS)中或被检测为继发性NBS紊乱。
除3-MGA-I外,其他四种遗传性疾病与尿液中过量排泄3-MGA有关,但都是由其他基因突变引起的:tafazzin缺乏引起的Barth综合征(3-MGA-II,MIM#302060),由未知蛋白缺乏引起的Costeff视神经萎缩综合征(3-MGA-III,MIM#258501),以及机制仍不清楚的3-甲基戊二酸尿症Ⅳ型和Ⅴ型。与其他MGA类型患者相比,3-MGA-I患者在尿液中排出的3-甲基戊二酸和两种代谢物3-MG和3-HIVA水平更高。所有这些疾病也可以通过NBS发现。
我们报道了一个由于新的AUH基因突变(纯合子变异体c.330+5G>a)引起的3-MGA-I女性患儿,最初表现为性早熟。
病例介绍
这名5.5岁的女孩因为有早熟的迹象,被送至卢布尔雅那大学儿童医院(UCHL),患儿从4岁开始逐渐乳房发育。她是第一个可能是非血缘关系的白人父母的孩子,在怀孕后的足月出生。她有一个兄弟姐妹患有1型糖尿病,家族史无其他早熟病例。母亲的月经初潮报告在13岁,父亲报告剃须在19岁。患儿无明显的围产期病史。她的早期发育正常,11个月时开始行走,无语言障碍。
患儿第一次就诊时,黄体生成素(LH)值升高(基础LH 0.2 IU/L,经GnRH 100μg/m2*体表面积刺激后,LH峰值为26.2 IU/L),骨龄显著提前(+3.5 SD),生长速度加快(就诊前6个月,她身高增加了6 cm),证实了患儿的中枢性早熟。此后,她每3个月定期接受GnRH激动剂曲普瑞林治疗,有效地阻止了青春期发育。6岁时,她做了脑部核磁共振以排除性早熟的主要原因。脑部核磁共振扫描显示,T2和FLAIR高强度病变位于半卵圆中心、双侧皮质下额叶白质和额顶叶深部白质,下丘脑和垂体未见明显变化。
由于核磁共振检查怀疑是缺血性病变,她被转诊到儿童神经科。6岁8个月时的神经系统检查显示中枢性张力减退、意图性震颤和膈肌收缩障碍。全身体格检查未见其他明显发现。由于在核磁共振成像上怀疑有缺血性病变,所以进行了一系列高凝状态检查,结果正常。心电图、超声心动图、经颅多普勒检查均正常。
患儿还进行了选择性代谢筛查,通过气相色谱-质谱(GC/MS)对尿液有机酸进行分析,发现3-MGA和3-HIVA水平较高。用串联质谱法(LC-MS/MS)对干血迹中的酰基肉碱进行分析,发现3-羟基异戊基肉碱(C5-OH)水平升高。其他代谢测试结果正常。
随后,对淋巴细胞中的3-MGH-酶活性进行了评估(在阿姆斯特丹大学医学中心进行了商业化测试),结果显示其水平极低(0.02 nmol/min/mg蛋白质;参考范围为1.4-4.6 nmol/min/mg蛋白质)。为了证实诊断,我们进行了AUH突变分析,在AUH基因中发现了一个新的纯合子变异c.330+5G>a。
在随访期间,患儿所有的测量提示3-MGA和3-HIVA升高。该患者的C5OH水平也升高(高于上限1.5-3.2倍;参考范围0-0.43μmol/L),总肉碱和游离肉碱水平正常。病人出生时,斯洛文尼亚没有进行NBS。检测卡逆行分析,结果未显示C5OH升高,这可以解释为卡片在室温下存放了5年多。
在确诊3-MGA-I后,在8岁时开始限制性亮氨酸饮食(60毫克/千克/天)和左旋肉碱补充(85毫克/千克/天)。
父母报告说,患儿在5岁时被确认患有注意力缺陷/多动障碍,8岁时在学校患有学习障碍。Beery-Buktenica视觉运动整合发展测试及伦敦塔测试(ToL)在8.5岁时由一位心理学家进行,结果显示患儿认知功能低下,视觉运动整合能力低,处理速度慢。在布朗儿童注意力缺陷障碍量表中,她表现出中度到中毒的问题。由于学习障碍,她被转到特殊教育学校。
9岁时重复脑部核磁共振检查显示双侧额叶皮质下白质和额顶叶深部白质高强度病变。采用阿司匹林保护(100毫克/天)。一年后进一步的脑部核磁共振成像显示先前描述的高强度病变没有明显变化(图1)。
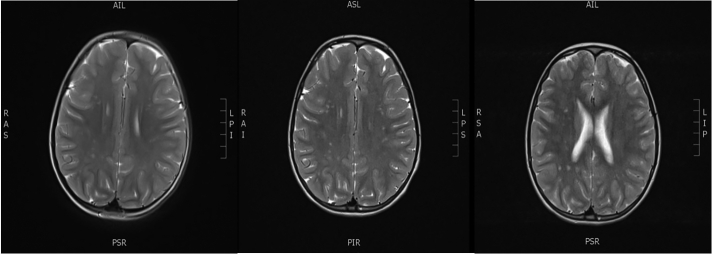
总结
综上所述,这是第一篇儿童中枢性性早熟的报告,可能与3-MGA-I有关。用促性腺激素释放激素激动剂曲普瑞林治疗能有效地阻止青春期发育。对这些特殊临床症状的认识有助于理解这种极为罕见的IEM的发病机制。另一方面,揭示性早熟IEM患者下丘脑参与的机制可能有助于对青春期调控的认识。
医博士编译自:Bizjak N, Tansek MZ, Stefanija MA, et al. Precocious puberty in a girl with 3-methylglutaconic aciduria type 1 (3-MGA-I) due to a novel AUH gene mutation. Molecular Genetics and Metabolism Reports. 2020; 25:100691. doi:10.1016/j.ymgmr.2020.100691.
参考链接:https://pubmed.ncbi.nlm.nih.gov/33304818/
声明: 所有注明“来源:医博士”的文字、图片和音视频资料,版权均属于医博士所有,转载须注明“来源:医博士”;所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。