微生物群可能通过生成可调节宿主炎症和代谢的咪唑丙酸而导致2型糖尿病
来源:医博士 | 2021-06-07 作者:刘雅丽
2型糖尿病是一种代谢性和社会性疾病,与肠道微生物群改变有关,其特征是产生丁酸盐的细菌数量较少。人类粪便微生物群转移实验已经证明肠道微生物群可以直接影响胰岛素敏感性,这提供了肠道微生物群可以促进疾病发展的因果证据。饮食强烈影响微生物的组成,并为微生物酶产生代谢产物提供底物,从而调节宿主生理。由于不同种族和不同地理区域的微生物组群不同,肠道微生物组衍生代谢物可能是比特定分类群更为保守的生物标记物。此外,代谢物可能提供疾病机制,以开发新的糖尿病治疗策略。
越来越多的数据表明,饮食成分的微生物代谢有助于心脏代谢疾病,但其之间的相互作用关系研究尚稀缺。一些细菌代谢产物如次生胆汁酸、短链脂肪酸、支链氨基酸和三甲胺等引起了人们对心脏代谢疾病的极大兴趣。我们最近发现,咪唑丙酸(ImP)是由2型糖尿病相关微生物通过组氨酸的交替代谢产生的,组氨酸通过激活p38γ-mTOR1-S6K1信号传导而导致糖代谢受损。
在这里,我们检测了来自三个不同欧洲国家的大型欧洲多中心队列(MetaCardis)中的ImP血清水平,该队列由不同程度的糖代谢受损的受试者组成,这表明ImP在糖尿病前期和2型糖尿病患者中升高。此外,我们扩展了以往的研究,以证明ImP与炎症、微生物群改变、饮食习惯有关,但与组氨酸摄入量无关。
MetaCardis队列中的2型糖尿病患者年龄稍大,与健康个体和糖尿病前期受试者相比,非白种人男性比例较高。患者的代谢状况受损(较高的体重指数(BMI)和腰臀比、血糖、胰岛素、糖化血红蛋白和血脂谱),而肾功能无明显差异。
与健康对照组相比,2型糖尿病前期和2型糖尿病患者的血清ImP水平显著升高(图1a),受试者种族背景无影响(补充图1a)。在所有登记中心也进行了类似的观察(补充图1b)。与ImP水平最低四分位的受试者相比,处于最高四分位的受试者患糖尿病前期[优势比(OR)为1.75;95%可信区间(CI)为1.18–2.57;P = 0.006]和2型糖尿病[OR 2.76,95%;CI 1.86–4.12,P < 0.001;图1b,c,补充表1,在调整传统风险因素(模型1:年龄、性别、BMI、种族)后]及肾功能损伤(模型2:模型1+肌酐清除率)的风险更高。
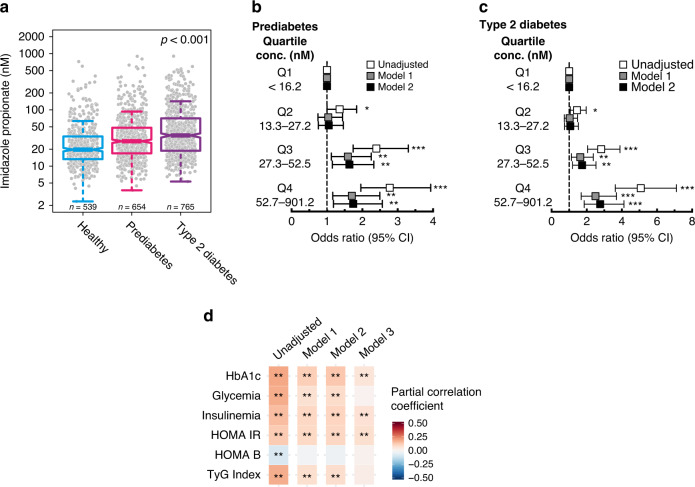
图1
接下来我们研究了ImP水平与糖脂代谢标志物以及胰岛素抵抗替代物之间的关系。ImP与空腹HbA1c、血糖、胰岛素血症、HOMA-IR和甘油三酯血糖指数呈正相关,与HOMA-B呈负相关。这些结果表明循环ImP与糖代谢受损之间存在联系。重要的是,在校正已知的传统危险因素(模型1:年龄、性别、BMI和种族)、肾功能(模型2:模型1+肌酐清除率),甚至存在2型糖尿病(模型3:模型2+糖尿病状态,图1d,补充表2)后,相关性仍然显著。
为了研究ImP是否也与糖代谢的动态评估相关,我们对进行口服葡萄糖耐量试验(OGTT)的亚群(n = 586)进行了进一步分析。基于ImP四分位数的受试者分层显示,ImP水平升高与OGGT后2小时血糖、胰岛素和C肽水平升高相关,转化为Stumvoll敏感性指数降低(补充表3)。
总之,血清ImP在糖尿病前期和2型糖尿病患者中升高,并与独立于糖尿病状态的糖代谢受损标志物相关。
二甲双胍是治疗2型糖尿病的一线药物,对微生物群的组成和功能有着深远的影响。ImP可改变二甲双胍的降糖作用。因此,我们评估了二甲双胍和其他抗糖尿病药物对ImP水平的影响(补充图1c)。二甲双胍治疗的2型糖尿病患者的ImP水平高于未经任何治疗的患者。这可能是由于二甲双胍治疗后微生物组发生了改变,或者反映了需要多药治疗的更严重的疾病表型。当我们进行一项仅包括未接受抗糖尿病治疗的受试者的子分析时,2型糖尿病受试者的ImP水平显著升高[28.1 nM(16.1–59.2)中位和四分位间距;n = 140]与糖尿病前期[27.8 nM(17–49.3)中位数和四分位数范围;n = 654]或正常葡萄糖耐量[19.7 nM(13.2–33.9)中位数和四分位数范围;n 359](P 0.028,调整年龄、性别、BMI、种族和肌酐清除率后的线性回归)。
当我们对存在心血管疾病(CVD)进行亚分析时,我们可以观察到,与没有心血管疾病的受试者[25.2 nM(15.2–47.7)中位数和四分位间距;n = 1568]相比,患有心血管疾病的受试者[36.7 nM(20.5–69.1)中位数和四分位间距;n = 390]的ImP水平显著升高,这需要进一步的研究(P <0.001,调整年龄、性别、BMI、种族、糖尿病状态和肌酸酐清除率后的线性回归)。
由于低微生物组基因计数与肥胖、胰岛素抵抗和血脂异常有关,我们接下来研究循环中ImP水平的增加是否与微生物组改变有关。因此,将研究人群分为高基因计数和低基因计数(阈值:607000个基因),观察到基因计数低的受试者与基因计数高的受试者相比,循环ImP水平更高,与糖尿病状态无关(图2a)。我们观察到ImP残差(根据年龄、性别、BMI、种族和肌酸清除率调整的ImP水平)和独立于糖尿病状态的基因计数之间存在显著的负相关。有趣的是,与糖尿病前期和健康受试者相比,2型糖尿病的影响范围更大(R = −0.31,P < 0.001)(补充图2a)。
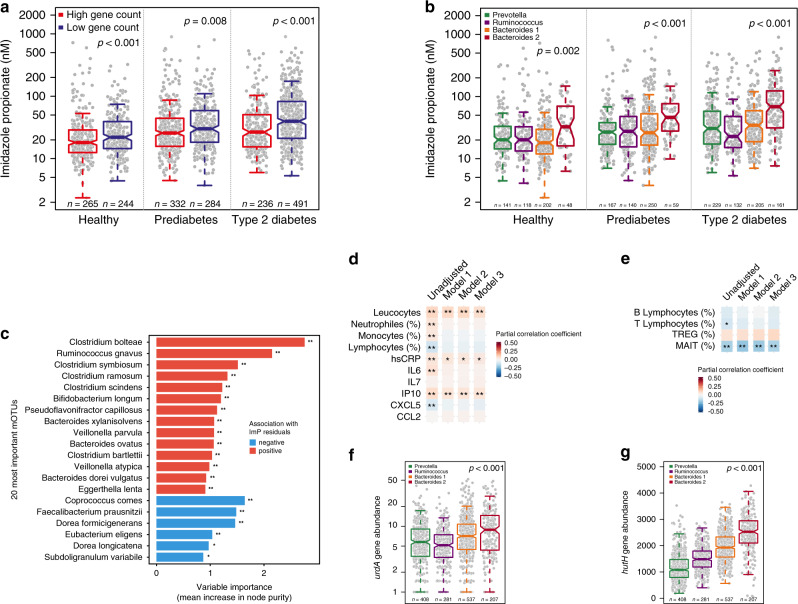
图2
人类肠道微生物群可分为群落型,也称为肠型。我们接下来分析了ImP水平是否与特定的肠型相关,并观察到类杆菌2肠型的受试者与其他肠型相比血清ImP水平显著升高(图2b)。这种肠型与低基因丰富度、低细菌细胞负荷以及代谢受损和炎症前疾病(如炎症性肠病)有关。接下来,我们用随机森林方法研究了特定mOTUs是否与ImP水平相关。我们观察到,在调整年龄、性别、体重指数、种族、肌酸清除率和糖尿病状况后,博尔特梭状芽孢杆菌、共生梭状芽孢杆菌和gnavus瘤胃球菌是与ImP正相关的最重要的致病菌(图2c和补充表4)。以前有报道称,代谢性疾病(如2型糖尿病和糖尿病前期)患者以及炎症性肠病(IBD)患者体内的细菌数量增加。与此相反,其他具有抗炎能力的细菌,如普氏粪杆菌与血清ImP水平呈负相关。综合这些数据表明,血清中的ImP水平与促炎微生物群的组成有关,这与ImP最初在肠道炎症患者中升高的观点一致。
接下来,我们在人群中探讨了ImP水平是否与炎症血清标志物相关,并观察到血清ImP水平与炎症血清标志物[总白细胞计数、高敏C反应蛋白(hs-CRP)、干扰素-γ诱导蛋白10(IP-10)]校正已知的传统危险因素(模型1:年龄、性别、BMI、种族)、肾功能(模型2:模型1+肌酐清除率)和2型糖尿病(模型3:模型2+糖尿病状态)呈正相关(图2d和补充表5)。
此外,通过检查具有外周血淋巴细胞特征的来自心包队列的亚群(n = 439),我们观察到ImP水平与循环黏膜相关不变T细胞之间存在显著的负相关(MAIT,图2e和补充表6),它们具有与生俱来的类似效应物的特性,可以抵御微生物感染。有趣的是,外周血MAIT细胞的减少与代谢性疾病和肥胖症有关,并与心内膜人群的心脏代谢性疾病进展有关。总的来说,低基因计数微生物群和类杆菌2型肠型与循环ImP水平增加相关,后者可能通过促进轻度炎症而导致2型糖尿病。
为了进一步了解微生物群如何将组氨酸代谢为ImP,我们分析了编码组氨酸解氨酶的hutH基因和编码尿苷酸还原酶的urdA基因的丰度。评估酶特异性的一个主要挑战是具有同源序列的几种酶可能具有不同的底物特异性。然而,urdA可以根据活性位点FAD结合域中的氨基酸进行鉴定。
urdA是一个低丰度基因,而hutH更为普遍,在201个宏基因组物种中观察到(补充表7)。
校正年龄、性别、BMI、种族和肌酐清除率后,根据糖尿病状态和ImP四分位数,hutH和urdA丰度均增加(补充图2b-e)。正如预期的那样,类杆菌2肠型的urdA和hutH丰度均增加(图2f,g)。与hutH和urdA丰度增加与类杆菌2肠型之间的关系一致,我们还观察到这些基因与基因丰富度之间的负相关(分别为hutH和urdA,rho −0.41,P < 0.001和rho −0.25,P < 0.001)(补充图2f,g)。
组氨酸是ImP的前体,因此,我们评估了研究人群的每日饮食组氨酸摄入量。根据食物频率调查问卷记录,当按ImP四分位数对人群进行分层时,我们没有观察到组氨酸摄入量的任何显著差异(图3a)。因此,我们没有观察到对照组和2型糖尿病受试者循环组氨酸水平的差异(n = 1895;P = 0.78)。接下来,我们评估了营养素摄入量的全谱,并确定ImP与饱和脂肪摄入量(由高奶酪摄入量驱动)之间存在显著正相关,与纤维和不饱和脂肪摄入量(由减少蔬菜和坚果摄入量驱动,图3b)之间存在负相关。此外,我们通过不同的指标/评分[替代健康饮食指数(aHEI)、阻止高血压的饮食方法(DASH)评分、饮食多样性评分(DDS)和地中海饮食评分]对更广泛的饮食模式进行了评估。校正年龄、性别、BMI、种族、中心(国家)、每日能量摄入、肌酐清除率和糖尿病状态后,ImP血清水平与aHEI、DSS和地中海饮食评分呈负相关。值得注意的是,这些关联的影响大小相对较小,但总体上表明不健康饮食与ImP水平增加有关(图3b)。
;
图3
总之,我们的数据表明,不健康的饮食可能导致微生物群落类型的改变,从而增加将膳食组氨酸代谢为ImP的潜力,进而通过激活MAPK信号导致胰岛素受体底物和炎症信号的降解,从而导致糖代谢受损。由于已观察到在不同原因的糖耐量和2型糖尿病患者中ImP增加,个性化饮食推荐或抑制urdA可能有助于降低循环ImP水平。
医博士编译自:Molinaro A, Bel Lassen P, Henricsson M, et al. Imidazole propionate is increased in diabetes and associated with dietary patterns and altered microbial ecology. Nature Communications. 2020; 11(1):5881. doi:10.1038/s41467-020-19589-w.
来源:https://pubmed.ncbi.nlm.nih.gov/33208748/
声明: 所有注明“来源:医博士”的文字、图片和音视频资料,版权均属于医博士所有,转载须注明“来源:医博士”;所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。