B7-H3 CAR-T治疗部分控制了基底细胞癌患者的肿瘤生长
来源:医博士 | 2023-05-08
嵌合抗原受体(CAR)-T细胞疗法在治疗造血恶性肿瘤方面取得了显著成功,包括CD19 CAR-T治疗B细胞急性淋巴细胞白血病(B-ALL)和BCMA CAR-T治疗多发性骨髓瘤(MM)。然而,同样的成功尚未在实体瘤中复制。其中一个挑战是确定CAR-T靶点,该靶点在实体瘤上特异表达,但在正常组织上不表达。
B7-H3(也称为CD276)是一种免疫检查点分子,在正常组织中无表达或低表达,但在胶质母细胞瘤、卵巢癌、非小细胞肺癌、鳞状细胞癌、黑色素瘤和其他恶性实体瘤中高表达。B7-H3已被证明有助于肿瘤转移,并且通常与不良的临床预后相关。基于这些发现,B7-H3被认为是癌症免疫治疗的一个有前途的靶点。B7-H3已显示在90%的皮肤癌上高度表达,包括黑色素瘤、基底细胞癌(BCC)和鳞状细胞癌(SCC)。对于原发性基底细胞癌,标准手术切除通常是一种合适的治疗选择。尽管基底细胞癌通常进展缓慢,但一小部分基底细胞可通过局部侵袭发展为转移性或局部晚期基底细胞癌(LaBCCs)。对于LaBCCs和复发性或不可切除的BCCs,系统治疗是必要的。然而,治疗引发的不良事件通常会导致治疗中断;因此,需要制定新的治疗策略。对于BCCs的治疗,尤其是LaBCCs,免疫疗法无疑是一个非常有前途的选择,例如使用PD-1阻断剂。尽管CAR-T在实体瘤中的临床应用仍然相对有限,但大量研究已经开始探讨其临床应用的有效性和安全性问题。目前还没有基于CAR-T的BCC免疫治疗的报告。
在此,本文报告了一例在过去10年中多次手术和治疗后复发的多发性基底细胞癌患者。通过肿瘤内注射三剂自体抗B7-H3 CAR-T细胞后,患者获得了部分反应,并出现了暂时和轻微的副作用。这项研究为B7-H3阳性恶性实体瘤患者提供了一种潜在的治疗策略。
病例介绍
2003年,一名65岁的男性患者被初步诊断为多发性基底细胞癌,皮肤检查显示患者前额和腹部有多个深色斑块或丘疹,较大的斑块显示溃疡和出血。异常皮肤组织的组织病理学显示栅栏状嗜碱性基底样上皮与相邻基质形成裂缝。此后,患者接受了多种化疗和手术。然而,疾病复发并蔓延到全身。一些病变,尤其是前额的大病变(6cm×6cm),伴有溃疡渗出物和疼痛,并且无法通过手术去除。患者要求替代治疗方案。
肿瘤组织的免疫组织化学染色显示B7-H3阳性,阳性率为80%,强度为++/+++(图1A);因此,患者参加B7-H3-CAR-T免疫治疗的临床试验。鉴于这是首次尝试用抗B7-H3 CAR-T细胞治疗患者以清除皮肤肿瘤,对患者进行了肿瘤内注射而不是静脉注射,目的是增加局部肿瘤区域CAR-T细胞的数量和浓度。进行了三次CAR-T注射。第一次肿瘤内注射CAR-T于2020年11月进行,第二次注射于2020年12月,第三次注射于2021年1月。
抗B7-H3的人源化单链可变片段(scFv)用于获得基于4-1BB的第二代CAR-T(图1B)。体外和体内测试了B7-H3-CAR-T细胞的肿瘤杀伤能力;所有结果表明CAR-T细胞在杀伤B7-H3阳性肿瘤细胞和控制荷瘤NSG小鼠模型中的肿瘤生长方面具有潜力。
为了保持免疫系统的完整,在CAR-T细胞注射之前,没有给患者进行淋巴消耗性化疗。在CAR-T治疗过程中,患者通过肿瘤内注射三次自体抗B7-H3 CAR-T细胞,并在第1天、第14天和第62天增加剂量(图1C)。该患者有两个不同的肿瘤部位接受治疗(腹部肿瘤的部位1为1.8 cm×0.6 cm;前额肿瘤的部位2为6 cm×6 cm)。制备两批CAR-T细胞用于注射,CAR转导率为52.50%和42.16%,CD4/CD8比值分别为3.25和1.89。使用FITC标记的重组B7-H3蛋白通过流式细胞术分析注射后外周血中CAR阳性T细胞的扩增和百分比。
在整个治疗过程中,在外周血中检测到非常低水平的CAR-T细胞。在第三次注射后的第5天,外周血中只有2.5%的T细胞为CAR阳性(图1D),2天后CAR-T细胞的百分比降至无法检测的水平(图1D,E)。
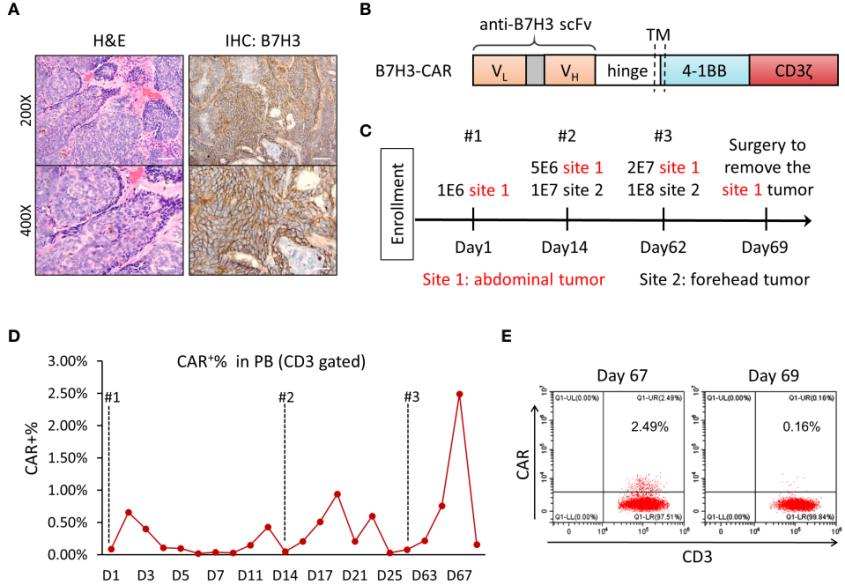
图1. 连续注射B7-H3 CAR-T细胞治疗的临床检查
第一次注射后,患者的丙氨酸转氨酶(ALT)和天冬氨酸转氨酶(AST)水平略微升高约两倍。在第6天达到峰值后,ALT和AST水平开始缓慢下降。在第二次和第三次注射后,没有观察到ALT和AST水平升高。治疗期间,患者血浆γ-谷氨酰转肽酶(γ-GT)和碱性磷酸酶(ALP)水平相对稳定。同时,CAR-T治疗期间血浆IL-6保持在较低水平。患者的体重在治疗期间保持稳定,没有任何与治疗相关的显著变化。CAR-T治疗期间的血常规检查没有明显异常,包括白细胞(WBCs)、中性粒细胞、血小板、淋巴细胞、单核细胞的细胞计数和血红蛋白浓度。
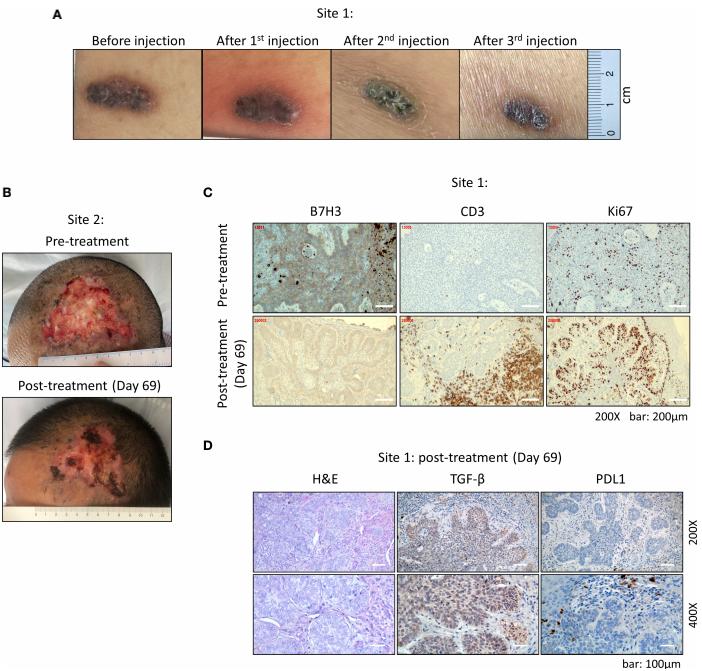
图2. CAR-T细胞治疗后多发性基底细胞癌的临床表现
三次注射后,腹部(部位1)的原始病变体积减小了40%(从1.8 cm×0.6 cm减小到1.3 cm×0.5 cm),从隆起变为扁平(图2A)。前额的大病变(部位2)由于最初的溃疡和出血而变得干燥(图2B)。第三剂CAR-T注射后,进行了手术切除腹部剩余的肿瘤。IHC分析表明,在第三次注射CAR-T细胞后,B7-H3阳性细胞的百分比从80%下降到约40%,并且B7-H3强度从++/+++下降到+(图2C)。同时,CD3 T细胞在肿瘤内的注射部位富集;然而,这些T细胞中的大多数未能渗入邻近的肿瘤区域,B7-H3和Ki67染色阳性(图2C)。随后,检查了两种常见抑制信号分子TGF-β和PD-L1的表达,并在CAR-T治疗后在肿瘤区域观察到TGF-β的高表达水平(图2D)。
最终,在B7-H3 CAR-T治疗后,部位1和2的肿瘤生长都得到了部分控制;然而,肿瘤并未完全根除。在随访中,患者的生理状况稳定,CAR-T注射后无后遗症,并持续对肿瘤皮肤进行常规非手术治疗。
结论
本病案报告一名基底细胞癌患者接受了抗B7-H3 CAR-T治疗,三次瘤内注射后肿瘤生长得到部分控制;同时,观察到轻微且可控制的副作用。这些临床结果可能表明抗B7-H3 CAR-T在治疗皮肤癌方面的巨大疗效,尽管这些数据仅来自一名患者。近期需要进行更大规模的队列研究,以进一步评估抗B7-H3 CAR-T治疗的有效性和安全性问题。
医博士编译自:Hu G, Li G, Wen W, et al. Case report: B7-H3 CAR-T therapy partially controls tumor growth in a basal cell carcinoma patient. Front Oncology. 2022; 12:956593. doi:10.3389/fonc.2022.956593.
声明: 所有注明“来源:医博士”的文字、图片和音视频资料,版权均属于医博士所有,转载须注明“来源:医博士”;所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。