在无药物联合使用诱发的毒性下联合使用泊沙康唑-环磷酰胺治疗宛氏拟青霉肺炎合并狼疮性肾炎
来源:医博士 | 2023-09-26
宛氏青霉菌是一种机会性霉菌,在免疫抑制的人类中引起肺部感染,通常用三唑类药物治疗。狼疮性肾炎是系统性红斑狼疮患者进行性肾脏疾病的主要原因,通常需要环磷酰胺为基础的治疗。三唑类药物与环磷酰胺共同给药具有挑战性,因为三唑类药物会增加环磷酰胺的浓度,从而加重环磷酰胺的毒性。在此描述了一个患有宛氏拟青霉肺炎并伴有狼疮性肾炎的患者,成功用泊沙康唑和棘球白素桥接中断治疗,以允许环磷酰胺治疗。该方案耐受性良好,无环磷酰胺毒性,并改善了真菌性肺炎和肾功能。
病例介绍
患者女性,43岁,2019年从巴西移民到美国,患有甲状腺功能减退症,未经治疗的潜伏性结核病感染(LTBI),以及系统性红斑狼疮,表现为关节痛和发热,间歇性使用羟氯喹和泼尼松治疗。患者有间歇性咳嗽、呼吸困难、肌痛和自觉发热史3个月。这些症状归因于系统性红斑狼疮发作,促使患者开始使用泼尼松(60mg/天;1mg/千克/天)。当症状持续时,患者胸片显示左肺上叶浸润,使用左氧氟沙星经验治疗并且停用泼尼松。出现症状4个月后,对患者行支气管镜检查,支气管肺泡灌洗液培养宛氏青霉菌阳性 (对受试抗真菌药物的最低抑菌浓度[MICs]为:两性霉素B ≤0.03μg/mL,伊曲康唑16μg/mL,伊曲康唑≤0.03μg/mL,伏立康唑4μg/mL,泊沙康唑≤0.03μg/mL,奥洛非姆0.25μg/mL;对米卡芬净的最小有效浓度[MEC]:≤0.015mg/ml)在MALDI-TOF上识别。德克萨斯州圣安东尼奥的真菌检测实验室对包括奥洛非姆在内的抗真菌药物进行了敏感性试验。开始使用伊曲康唑(每12小时200mg)并持续使用羟化氯喹。两周后胸部电脑断层扫描(CT)显示左上肺叶持续实变和肿块样阴影。患者随后被转介到美国国立卫生研究院。
实验室分析显示白细胞计数正常(4760cells/μL),低钾血症(3.2mmol/L),C反应蛋白为8.0mg/L。血清肌酐为0.99mg/dL,估计肾小球滤过率(eGFR)为70ml/分钟/1.73m2(详细的实验室数值见表1)。停用伊曲康唑,开始使用泊沙康唑(300mg/天)。患者在上个月出现了新发高血压(最大血压,179/111mmHg)。胸部CT显示左上肺叶实变和一个1.8cm的结节,在正电子发射断层扫描(PET)/CT扫描中显示为氟脱氧葡萄糖(FDG)阳性,伴有PET阳性的左腋窝和胸廓下淋巴结病(图1A)。鼻窦CT无明显异常。
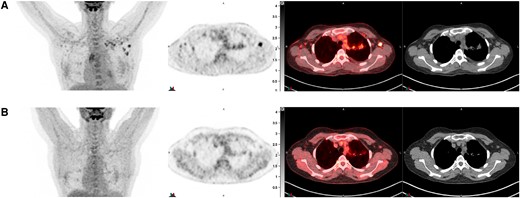
图1、患者胸部的PET/CT A从左至右,冠状最大密度投影图像、轴位PET、PET/CT叠加和轴位CT扫描,从伊曲康唑转换为泊沙康唑治疗后约1周。B6个月后,在环磷酰胺的第六个周期时,相同的图像序列
考虑到低钾血症和新发高血压,医生怀疑伊曲康唑引起的假性醛固酮增多症是由三唑类药物作用引起的盐皮质激素代谢异常引起的,其特征是在低血清肾素活性和醛固酮的情况下盐皮质激素过多。这被11-脱氧皮质醇水平为498 ng/dL,醛固酮(< 3.0 ng/dL)和肾素(< 0.6 ng/dL) 证实,为此开始服用螺内酯和补钾。尿液研究显示肾病范围的蛋白尿(点蛋白与肌酐的比率,5216mg/g;24小时尿蛋白排泄量,5.324克),考虑为狼疮性肾炎。血清C3和C4分别为70和16mg/dL。蛋白尿程度以及低白蛋白血症和尿沉渣检查中脂肪脂滴的存在符合肾病综合征。
患者接受了经皮肾活检,结果显示在受检肾小球中存在25%的弥漫性增生型球样硬化,在8个剩余肾小球中的7个中存在坏死性和硬化性新月体,符合IV类(弥漫性增生)和V类(膜性)狼疮肾炎(图2)。考虑到进展为终末期肾病的严重性和高风险,开始使用羟氯喹,即甲基强的松龙(1g/天)静脉注射3天,然后口服泼尼松(40mg/天;0.67mg/千克/天)逐渐减量,静脉注射环磷酰胺750mg/m2给药,按月给药,持续7个月。此外,患者开始使用异烟肼治疗LTBI,并使用阿托伐酮预防肺孢子虫。
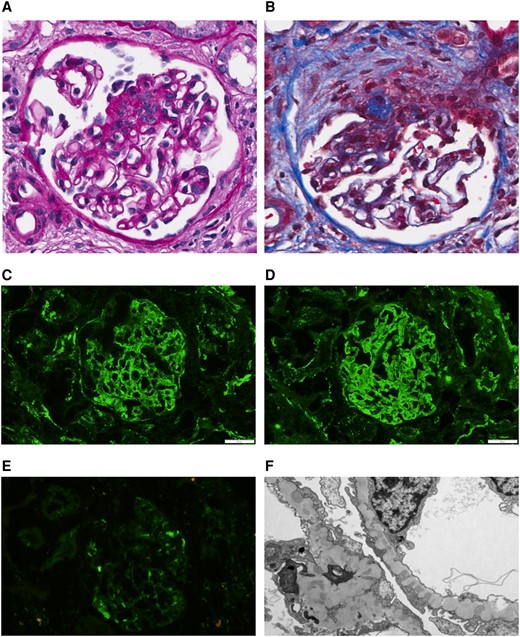
图2、组织学发现符合患者的严重狼疮性肾炎。高碘酸希夫(A)和马森三色(B)在用糖皮质激素和环磷酰胺治疗之前,患者的肾活检染色显示出细胞过多和增生,以及涉及鲍曼囊和肾小球簇的纤维细胞新月体。荧光免疫组织化学染色进一步显示弥漫性C3(C)和免疫球蛋白G(D)在整个肾小球的沉积以及C1q的低强度染色(E).电子显微镜(F)显示膜内和上皮下免疫沉积,具有来自肾小球基底膜的尖峰投射
由于担心环磷酰胺和泊沙康唑之间的相互作用,并考虑到需要用基于环磷酰胺的疗法治疗狼疮性肾炎,但考虑到泊沙康唑和环磷酰胺的半衰期分别为15-25小时和5.5小时,医生计划在环磷酰胺给药前3天和给药后1天继续使用泊沙康唑。泊沙康唑留用4天期间,给予患者米卡芬金(150mg/天)治疗,以提宛氏拟青霉覆盖,同时给予大剂量强的松治疗,以尽量减少真菌感染恶化的风险。该方案使用环磷酰胺周期超过7个月,患者未出现环磷酰胺毒性,即骨髓抑制、心脏毒性、肝毒性或出血性膀胱炎。泊沙康唑基线谷浓度在持续使用泊沙康唑前为1810-4010 ng/mL,在每次环磷酰胺给药前为81-583 ng/mL,服用环磷酰胺后第二天,泊沙康唑重新开始治疗时为< 50-296 ng/mL(图3)。在环磷酰胺第4周期前的治疗因主观发热、疲劳增加和转氨酶轻度升高与巨细胞病毒(CMV)再激活相关(病毒载量,6.02 log10IU/mL(全血的聚合酶链式反应[PCR]),同时接受15 mg泼尼松/天。患者接受了口服缬更昔洛韦(450 mg,每天两次)治疗4周,症状迅速缓解。在接下来的环磷酰胺周期复查时,CMV PCR未检测到。
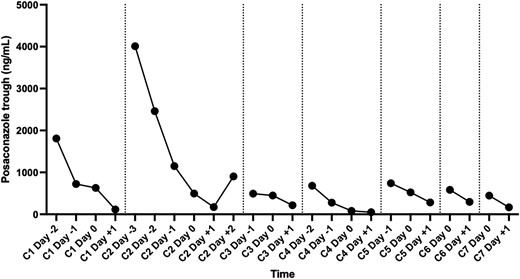
图3、环磷酰胺给药7个周期的泊沙康唑水平。此处显示的是在环磷酰胺每个周期前后测得的泊沙康唑水平。显示了环磷酰胺周期的编号(即C1-C7)以及相对于接受环磷酰胺的日期的日期(即第0天是接受每个环磷酰胺剂量的日期)
在患者接受环磷酰胺的第六个周期时,再次进行胸部PET/CT检查,显示实变和FDG亲和力有所改善(图1B)。到第七个周期时,尿蛋白与肌酐的比率提高到818mg/g(图4),C3和C4水平正常化。到了第七个周期血清肌酐峰值为1.46mg/dL(表皮生长因子受体,43mg/分钟/1.73m2)并提高到0.76 (eGFR,95mg/分钟/1.73m2)。低钾血症和高血压通过治疗狼疮性肾炎和用药从伊曲康唑转为泊沙康唑而得到解决,允许停止补钾和服用螺内酯。
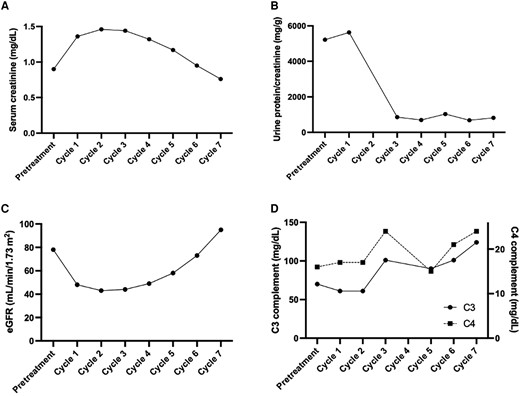
图4、以环磷酰胺为基础的治疗改善我们患者的狼疮性肾炎。基线时和环磷酰胺7个周期期间指示实验室值的纵向演变。显示了尿蛋白/肌酸酐比率(A),血清肌酐(B),通过估计肾小球滤过率(eGFR)计算的肾小球滤过率(C),以及补体蛋白C3和C4(D)
讨论
环磷酰胺给药的三唑类药物治疗的最佳中断时间是未知的。根据药物的半衰期和积极治疗这两种疾病的愿望选择了这里提出的时间;然而,保持三唑类药物更长治疗时间可能会进一步降低环磷酰胺毒性的风险,而不损害真菌感染的治疗效果。重要的是,该方案的安全性可能不适用于需要更高剂量或每日给药的其他适应症的环磷酰胺方案。不同患者之间泊沙康唑的不同代谢也可能需要改变泊沙康唑的持续时间。建议在服用环磷酰胺前,在保持药物的同时测量泊沙康唑的水平,以确保其水平足够低。此外,棘白菌素桥接抗真菌治疗的作用需要进一步研究。鉴于棘白菌素的耐受性,这被认为是一种低风险的干预措施,可将抗真菌治疗失败的风险降至最低。然而,由于宿主对棘白菌素的反应不同,因此很难将这种方法的成功推广到所有情况、病原体(例如甚至密切相关的真菌的易感性),以及药代动力学因素(如组织特异性药物渗透),因此最佳疗法必须根据具体情况而定。
医博士编译自:Pechacek J,Webb T,Ferré EMN, et al. Successful Treatment of Paecilomyces variotii Pneumonia and Lupus Nephritis With Posaconazole-Cyclophosphamide Co-administration Without Drug Interaction-Induced Toxicity. Open Forum Infectious Diseases. 2023; 10(8):ofad410. doi:10.1093/ofid/ofad410.
声明: 所有注明“来源:医博士”的文字、图片和音视频资料,版权均属于医博士所有,转载须注明“来源:医博士”;所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。