免疫检查点抑制剂治疗后血糖正常的糖尿病酮症伴肾上腺皮质功能不全的二型糖尿病合并肺癌
来源:医博士 | 2024-05-13
抗程序性细胞死亡(PD-1)、其配体(PD-L1)或细胞毒性T淋巴细胞抗原-4(CTLA-4)单克隆抗体的免疫检查点抑制剂(ICIs)已被批准为抗癌药物。它们被广泛用作几种晚期包括非小细胞肺癌(非小细胞肺癌)在内的恶性疾病的有效治疗方法。然而,ICIs可能导致免疫相关不良事件(irAEs),包括垂体功能减退、原发性肾上腺功能不全、甲状腺功能障碍、甲状旁腺功能减退和1型糖尿病。使用抗PD-1和抗CTLA-4抗体进行联合治疗时,内分泌irAEs的发生频率增加。
钠葡萄糖转运蛋白2抑制剂(SGLT2抑制剂)是一种新型降糖药物。它们可以通过抑制近端小管的重吸收和促进尿糖排泄来降低血糖。SGLT2抑制剂广泛用于二型糖尿病糖尿病(T2DM)的临床治疗。然而,SGLT2抑制剂也可能导致血糖正常的糖尿病酮症。这是一种危及生命的紧急情况,其特征是血糖水平<200 mg/dL的轻度高血糖症,伴有严重的代谢性酸中毒。血糖正常的糖尿病酮症酸中毒也可由其他因素诱发,如手术、创伤、妊娠、热量摄入减少、大量饮酒、入院前使用胰岛素或肝硬化。然而,在T2DM没有正常血糖的糖尿病酮症与irAEs诱导的单独ACTH缺乏相关的报道。在本病例报告中,描述了T2DM irAE相关血糖正常的糖尿病酮症的临床特征。
病例介绍
患者男性,74岁。58岁时患有T2DM。接受了总日剂量为0.58单位/kg/天的基础剂量胰岛素、100mg/天的卡格列净、1mg/天的格列美脲、1000mg/天的二甲双胍和0.75mg/周的度拉糖肽治疗。血糖控制不佳,糖化血红蛋白水平为8.0–9.0%。饮食以碳水化合物为主。患有脂肪肝。体重为79kg,体重指数为25.8kg/米2。空腹血清C肽水平为0.76-1.57 ng/mL,餐后C肽水平为2.25-6.28ng/mL,表明胰岛素分泌正常至轻度减少。
患者在公司提供的定期体检中发现了异常肺部肿块,被诊断为左下叶鳞状细胞癌(临床TNM分期T3N3M0和非小细胞肺癌分期IIIC)。随后接受了卡铂、紫杉醇、纳武利尤单抗(抗PD-1抗体)和易普利姆玛(抗CTLA-4抗体)治疗。定期给予纳武利尤(纳武)单抗和易普利姆玛(伊匹单抗)进行维持治疗。
在纳武单抗和伊匹单抗第3周期的第8天,患者感到全身乏力,白天嗜睡,食欲不振。在第13天,这些症状进一步恶化,停止注射胰岛素和度拉糖肽并服用所有口服降糖药。在第19天,因38.3°C的高烧和格拉斯哥昏迷评分(E4V3M5)评估意识水平低下被送到文章发表医院的急诊室。
入院时,患者血压、脉搏和呼吸频率分别为118/79mmHg、130次/分钟和24次/分钟。室内空气经皮血氧饱和度为97%。实验室验血和验尿结果如下:血清葡萄糖,121mg/dL;糖化血红蛋白,9.3%;乙酰乙酸2076 μmol/L;β-羟基丁酸,4995 μmol/L;尿酮体(3+);静脉血气pH值为7.40;C反应蛋白,16.6 mg/dL(表1)。非对比增强计算机断层扫描显示他的身体器官没有感染迹象。基于这些发现,诊断出血糖正常的糖尿病酮症。
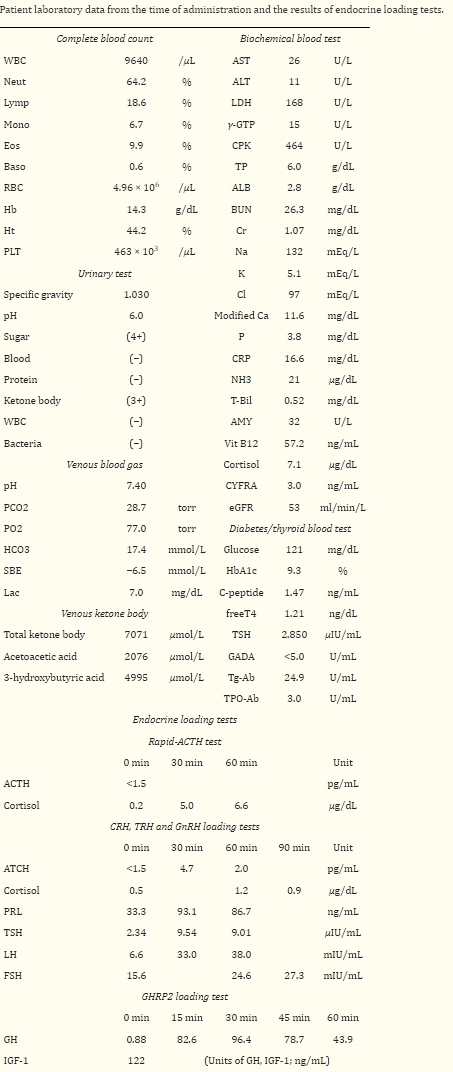
表一、患者给药时的实验室数据和内分泌负荷试验结果
患者接受了含葡萄糖、胰岛素和抗生素治疗的静脉补液,这是血糖正常的糖尿病酮症和细菌感染的标准治疗方法。但在住院第3日出现严重意识不清和低血容量性休克。3组血、尿液培养试验均为阴性。因此,怀疑患者为血糖正常的糖尿病酮症伴有肾上腺功能不全。开始连续5天静脉补充氢化可的松(80-150mg /天),然后每天两次口服氢化可的松补充(30mg /天)。患者病情明显好转,住院第7天尿酮体浓度为阴性。第8天进行快速ACTH试验以确认肾上腺功能不全的诊断(表1)。
随后,第10天进行促肾上腺皮质激素释放激素负荷试验,发现继发性肾上腺功能不全。其他垂体前叶激素水平正常(表1)。垂体增强和动态磁共振成像未见垂体或垂体柄肿大、肿块形成或炎症。确定了孤立ACTH缺乏症的诊断。临床医生判断这是一种irAE,并认为糖尿病酮症是继发性诱发的。根据不良事件通用术语标准v5.0 (CTCAEv5.0),患者的irAE评分为4级,即最严重或危及生命。患者在2个月内体重减轻了6.2公斤。患者于第23天出院,同时给予氢化可的松治疗。糖尿病通过基础胰岛素和每周注射胰高血糖素样肽-1受体激动剂治疗得到很好的控制(图1)。
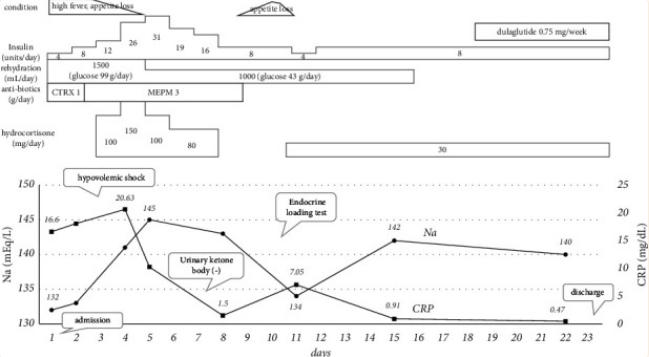
图1、入院后的临床追踪。CTRX、头孢曲松钠水合物;MEPM美罗培南水合物
讨论
这里报道了一例T2DM和非小细胞肺癌患者的病例,该患者患有血糖正常的糖尿病酮症和肾上腺皮质激素缺乏症。这是第一个报告的病例,在该病例中,正常血糖糖尿病酮症伴肾上腺功能不全的T2DM患者被确认为具有残余胰岛素分泌。迄今为止,已有三份报告将糖尿病酮症酸中毒伴孤立性促肾上腺皮质激素缺乏症视为一种irAE。所有患者均患有1型糖尿病并伴有单独的促肾上腺皮质激素缺乏。也就是说,在这些患者中,糖尿病酮症酸中毒是在绝对胰岛素缺乏的背景下发生的。然而,在本病例的患者中,正常血糖的糖尿病酮症患者的胰岛素分泌能力保持不变。
有几个临床因素被认为会导致胰岛素分泌残留的T2DM患者出现血糖正常的糖尿病酮症。与irAE相关的单独ACTH缺乏可能为血糖正常的糖尿病酮症提供了机会。然而,仅这一点不足以导致糖尿病酮症的发展,因为它不会导致胰岛素缺乏。除了与irAE相关的单独ACTH缺乏外,胰岛素注射和胰岛素促泌剂、SGLT2抑制剂的自我暂停以及碳水化合物摄入不足也可能导致血糖正常的糖尿病酮症的发生。接下来,我们详细描述了我们患者血糖正常的糖尿病酮症的发病机制(图2)。
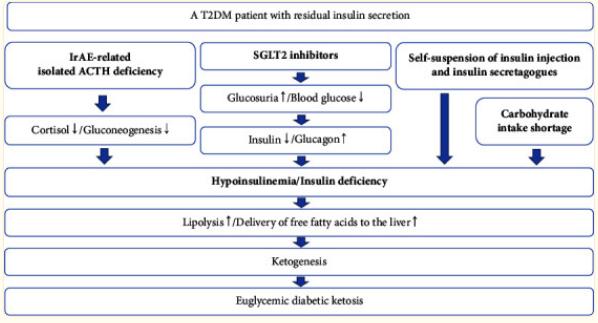
图2、血糖正常的糖尿病酮症发展示意图
胰岛素注射和胰岛素促泌剂的自我暂停可能加速了胰岛素缺乏。像往常一样控制血糖患者则需要大剂量胰岛素加胰岛素促泌剂。在生病期间,由于胰岛素敏感性降低,对胰岛素的需求增加。连续六天的自我暂停肯定会促进胰岛素缺乏。
肾上腺功能不全、SGLT2抑制剂和碳水化合物摄入不足可能会使血糖水平保持在较低水平。皮质醇在刺激糖异生和抑制糖原生成以防止低血糖中发挥作用。因此,肾上腺功能不全会导致低血糖症。SGLT2抑制剂通过抑制近端小管对葡萄糖的重吸收和促进尿葡萄糖排泄来降低血糖水平。在T2DM,以100毫克/天的剂量反复服用卡格列净的半衰期为11.8±3.2小时。然而,据报道SGLT2抑制剂的长期影响和正常血糖糖尿病酮症酸中毒的延迟恢复,甚至在6-10天内。Uenishi等人报告称,脱水和肾功能下降是SGLT2抑制剂长期影响的原因之一,我们的患者也显示了这一点。碳水化合物是葡萄糖的主要来源,众所周知,限制碳水化合物的饮食会降低血糖水平。本病例患者在血糖为102 mg/dL时空腹血清C肽水平为0.76 ng/mL的医疗记录。因此,肾上腺功能不全时胰岛素分泌受到抑制。
综合来看,起初,胰岛素注射和胰岛素促泌剂的自我暂停导致胰岛素相对缺乏,从而导致酮体的产生增加。其次,尽管胰岛素缺乏,肾上腺功能不全、SGLT2抑制剂和碳水化合物摄入不足仍使血糖水平保持在较低水平。最后,胰腺β细胞无法补偿胰岛素分泌的减少,导致暂时性严重胰岛素缺乏。暂时严重的胰岛素缺乏会促进脂肪分解、游离脂肪酸向肝脏的输送、生酮,并最终导致血糖正常的糖尿病酮症(图2)。
除了暂时性严重胰岛素缺乏外,胰高血糖素分泌的上调也导致酮体的过度产生,尽管未测量血清胰高血糖素水平。SGLT2抑制剂的给药刺激胰高血糖素的分泌,这是由胰岛素分泌减少介导的或SGLT2抑制剂对胰腺的直接作用α-细胞。
本病例患者因低胰岛素血症而出现糖尿病酮症,但不是糖尿病酮症酸中毒。McNulty等人报道了一例新诊断的1型糖尿病合并Addison病,该病仅表现为糖尿病酮症,未进展为糖尿病酮症酸中毒。Sheung等人报道称,患有阿狄森病的1型糖尿病患者自行停止胰岛素注射导致的糖尿病酮症酸中毒的酸中毒程度非常轻微。据推测,这是由于胰岛素缺乏导致的酮体合成被肾上腺功能不全部分抵消。
小结
总之,在此报告了一例T2DM患者,该患者因非小细胞肺癌而接受ICIs治疗,并因多种临床因素发展为血糖正常的糖尿病酮症。医疗专业人员有必要认识到这类患者发生血糖正常的糖尿病酮症的风险很高。
医博士编译自:Shibasaki S, Noda C, Imagawa A, et al. A Case of Type 2 Diabetes Mellitus with Lung Cancer Suffered from Euglycemic Diabetic Ketosis Accompanied by Adrenal Insufficiency after Immune Checkpoint Inhibitors. Case Reports in Endocrinology. 2024; 2024:9982174. doi:10.1155/2024/9982174.
声明: 所有注明“来源:医博士”的文字、图片和音视频资料,版权均属于医博士所有,转载须注明“来源:医博士”;所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。