家族病例:主要表现为早发性心脏瓣膜病分离与非典型早衰的LMNA基因变异
来源:医博士 | 2024-05-22
LMNA-基因编码中间丝核包膜蛋白的两种异构体,核纤层蛋白A和核纤层蛋白C。核纤层蛋白对几种细胞功能和中间丝核包膜蛋白的不同突变很重要LMNA-基因会导致一系列“层粘连病”。这些层板病通常分为四个表型组:(1)主要影响脂肪组织,导致脂肪营养不良;(2)影响外周神经,导致2型Charcot-Marie-Tooth病;(3)横纹肌病,导致肌肉营养不良和/或扩张型心肌病(DCM);以及(4)以过早衰老迹象为特征的类老年疾病,包括生长障碍、脱发和皮下脂肪减少。
超过400种致病变种LMNA-基因被报道了。心脏的LMNA相关疾病通常由DCM、(进行性)传导系统紊乱和心律失常组成,以常染色体显性模式遗传。扩张型心肌病可以是孤立的,但心外横纹肌也可以受累,如Emery-Dreyfuss肌营养不良症(EDMD)和肢带型肌营养不良症(LGMD)所示。核纤层蛋白A也被认为是调节衰老过程的重要蛋白质,因此,一些LMNA-基因变异可导致多系统早衰症,如Hutchinson-Gilford早衰综合征(HGPS)和沃纳综合征。还观察到了比经典HGPS综合征或沃纳综合征更不典型的类早衰表型。
在当前的病例系列中,描述了两个家族,在主要是主动脉瓣和二尖瓣过早钙化和狭窄的患者中,发现了两个新的LMNA基因变异,都位于外显子2。这些发现表明LMNA在这些家族中的基因变异携带者表现出主要影响心脏的非典型类早衰表型,而没有多系统受累的明确证据,这说明了层粘连蛋白A/C在不同疾病中的复杂作用。
病例介绍
家族1
家族1的(遗传疾病研究中家系的)先证者是一名62岁的男性,因主动脉瓣和二尖瓣过早钙化和功能障碍而就诊于临床遗传学家,并有心脏瓣膜病家族史。然而,患者心血管病史始于25岁时偶然发现的心脏杂音。经胸超声心动图显示严重的主动脉瓣狭窄,为此进行了同种主动脉瓣移植术;44岁时,由于中度至重度主动脉反流,采用主动脉瓣生物假体替代同种移植物,包括主动脉根(多伦多根)。手术期间,外科医生还必须对左心室流出道(LVOT)和二尖瓣前叶进行脱钙处理。53岁时,由于二尖瓣严重钙化,出现了严重的二尖瓣反流和狭窄,为此接受了瓣膜置换(机械假体)。在同一过程中,由于中度反流,进行了三尖瓣修复。图1显示了严重二尖瓣钙化的超声心动图图像,包括瓣环和瓣叶。不幸的是,因为原生主动脉瓣在30多年前被替换了,这个瓣膜的图像无法获得。除心脏瓣膜问题外,患者心脏病史包括心绞痛和急性冠状动脉综合征背景下的冠状动脉疾病,接受了多次血运重建手术,其中在39岁第一次经皮介入手术;44岁时同时进行了冠状动脉旁路移植术。此外,患者出现左心室收缩功能降低(缺血性)、房性心律失常、左束支传导阻滞和有症状的Mobitz II型传导阻滞,具有双心室起搏器适应症。
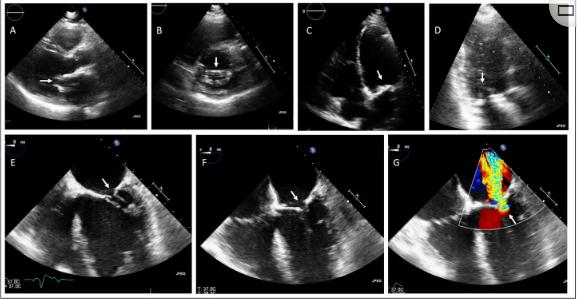
图1、家族1先证者的经胸(A-D)和经食管(E-G)超声心动图检查显示二尖瓣狭窄,主动脉瓣生物假体(多伦多根)原位。(A)胸骨旁长轴位,(B)胸骨旁短轴位,(C)根尖4室位,(D)根尖3室位,显示严重的二尖瓣钙化(箭头)。(E)食管中部舒张期和(F)收缩期,包括(G)彩色多普勒,显示二尖瓣狭窄和反流(箭头)
有趣的是,体格检查没有显示出系统性早衰症、脂肪营养不良或神经肌肉表型的特征。心脏疾病相关基因的全外显子组测序(WES)显示了心脏疾病相关基因的变异LMNA-基因(NM_170707.4 c.412G>C p.(Glu138Gln))。这种变异不存在于基因组聚合数据库(GnomAD v4.0.0)或英国生物库的参考等位基因中。它影响一种高度保守的氨基酸,蛋白质预测程序预测了一种致病作用(REVEL: 0.73)。基于这些发现,该变体被归类为意义不确定的变体(VUS; PM2_M; PP3_S)。
在将指标提交给临床遗传学家之前,对患者的家庭成员进行的心脏检查显示,其中几个家庭成员存在主动脉瓣和二尖瓣狭窄,包括(1)母亲(图2,II.2);(2)姐姐和她的儿子(图2III.1, IV.3);(3)姑姑(他母亲的姐妹)和她的女儿(图2、II.4, III.9)。与此同时,受影响的姐姐的另一个儿子(图2,IV.4),受影响阿姨的儿子(图2III.8)和另一个阿姨(母亲方,图2II.5)也患有心脏瓣膜疾病,但无法通过医疗记录证明这一点。然而,根据现有数据,瓣膜狭窄的诊断年龄应在25岁至(最大)53岁之间。先证者母亲的瓣膜外病史(图2、II.2)包括植入起搏器治疗房室传导障碍,而先证者的姐妹(图2III.1)出现阵发性房颤和冠状动脉疾病。总的来说,现有的超声心动图数据或所有患者的临床表现都没有提示风湿性病因的迹象。
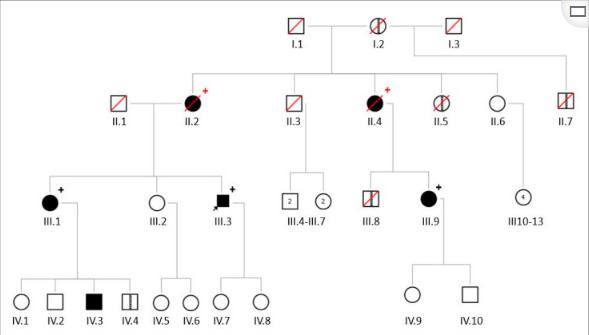
图2、家族1的家谱,黑色圆圈和正方形表示受影响的个体,白色圆圈和正方形表示未受影响的个体。圆圈或正方形中的条纹线表示患有失忆症的个体。圆圈=女性;正方形=男性;红色对角线=死者;箭头指向先证者;黑色加号= LMNA基因存在c.412G>C p.(Glu138Gln)杂合变异体;红色加号=该变体的专用载体
除了先证者之外,还检测了个体III.1和III.9,它们是LMNA-基因变异。这意味着,尽管不可能检测受影响的个人II.2和II.4,但他们是LMNA-基因变异。
家族2
在第二个家族中,先证者是一名34岁的男性,在一次与工作相关的医疗筛查中发现心脏杂音后,被诊断为严重的主动脉瓣和二尖瓣狭窄以及临界左心室肥厚,心脏收缩功能保留。在诊断时,先证者仅表现出疲劳症状,但没有特定的心脏相关症状(即气短、外周水肿、胸痛或心悸)。图3显示经胸超声心动图图像,显示主动脉瓣(三尖瓣)(图3C,D)和二尖瓣环和小叶(图3A、B、E)。诊断后,患者接受了主动脉瓣和二尖瓣联合置换术。术后因三度房室传导阻滞植入了起搏器。患者因年轻时患有心脏瓣膜病和心室肥大以及心脏瓣膜病家族史而被转诊至临床遗传学家处。体检时,没有观察到系统性前体细胞受累的迹象。全面的身体和实验室评估也显示该患者没有脂肪营养不良或神经肌肉受累的迹象。
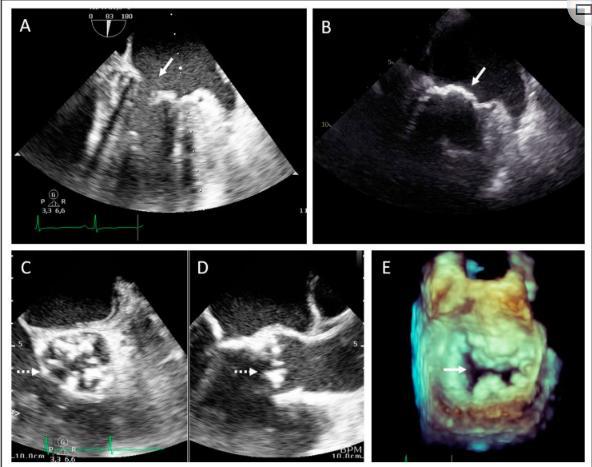
图3、家族2的先证者经食管超声心动图检查显示主动脉瓣狭窄和二尖瓣狭窄。(A,B)食道正中2室观显示严重的二尖瓣钙化(箭头)。(C)食管正中主动脉瓣短轴观和(D)长轴观,显示主动脉严重钙化(虚线箭头)。(E)舒张期二尖瓣三维数据显示明显钙化和狭窄(箭头)
对该家族的调查显示,先证者的兄弟姐妹分别在38岁和40岁时(图4、II1–II3)和他们的父亲(图4、I1)患有心脏瓣膜病。父亲(图4、I1)也患有主动脉瓣和二尖瓣狭窄,为此在55岁时进行了主动脉瓣置换术。左心室尺寸正常。姐姐(图4、II.1)和其中一个兄弟(图4、II.2)也具有主动脉瓣和二尖瓣狭窄,并伴有左心室向心性肥大。弟弟的超声心动图图像显示在图5A–E .根据现有超声心动图数据或该家族成员的临床表现,没有迹象表明瓣膜性心脏病的风湿性病因。
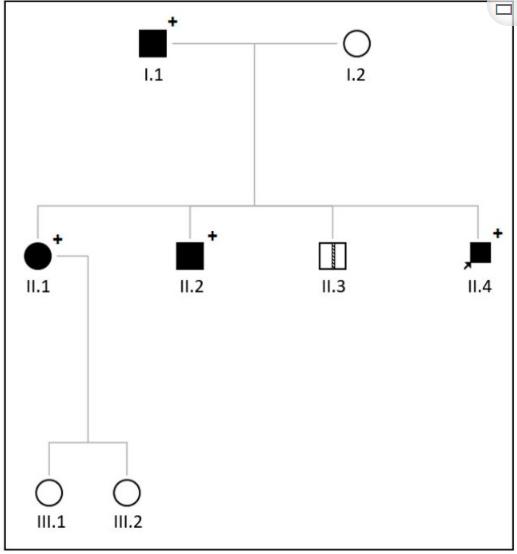
图4、家族2家谱黑色圆圈和正方形表示受影响的个体,白色圆圈和正方形表示未受影响的个体。正方形中的条纹线表示患有失忆症的个体。圆圈=女性;正方形=男性;箭头指向先证者;在LMNA基因中存在c.434A>G p.(Glu145Gly)的杂合变异
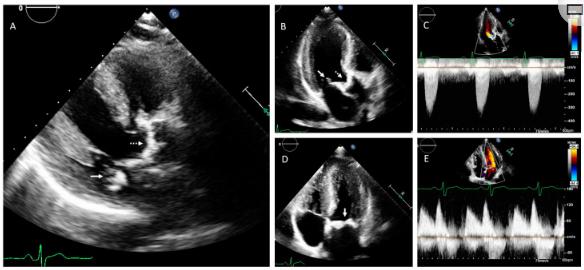
图5、家族2中II2的经胸超声心动图检查显示主动脉瓣狭窄和二尖瓣钙化。(A)胸骨旁长轴位,(B)顶三腔位,(C)主动脉瓣上连续波多普勒显示主动脉钙化和狭窄(虚线箭头)。(D)尖顶4室视图,(E)二尖瓣连续波多普勒,显示二尖瓣钙化和狭窄(连续箭头)
先证者的WES分析显示为杂合子LMNA-基因变体(NM_170707.4c.434 a》G.p .(Glu 145 Gly)。与家族1中的VUS相似,该变体在GnomAD v4.0.0和英国生物库参考数据库中不存在,并被预测具有致病作用(REVEL: 0.764)。受影响的父亲、兄弟和姐妹(图4I。1、II.1、II.2)也针对该特异性进行了测试LMNA-基因变异体和均被发现为杂合子携带者,表明变异体与表型分离。
讨论
突变LMNA-基因导致多种疾病,从孤立性扩张型心肌病到严重的系统性早衰症,如HGPS病。在这项研究中,描述了两个家族以前没有报道的变异LMNA-与孤立的过早严重心脏瓣膜钙化和疾病相关的基因共分离。虽然家族1的先证者也表现出冠状动脉疾病的特征,但在所有受影响的家族成员中一致的主要表型是主动脉瓣和/或二尖瓣过早狭窄。有趣的是,没有一个患者表现出系统性的类早衰、肌肉营养不良或脂肪营养不良表型。
关于瓣膜钙化的遗传作用的知识仍然难以捉摸。然而,最近的文献表明瓣膜钙化与甘油三酯水平升高的遗传倾向有关,而且与apoB、ACE、IL和LPA基因多态性以及IL1F9附近的遗传变异有关。据目前所知,具体的LMNA在这两个家族中观察到的基因变异以前没有在文献中描述过,也从未与严重的瓣膜钙化相关。
与家族1中发现的变体(p.Glu138Gln)相同位置的不同氨基酸变化(p.Glu138Lys: rs267607649,不存在于GnomAD v4.0的参考等位基因中)已在三份先前的病例报告中进行了描述。在所有这些报告中,描述了具有非典型HGPS表型的患者。与当前病例系列中描述的家庭不同,这些表型涉及儿童全身老化的特征。最值得注意的是Doubaj等人描述了一名11岁的女孩,其具有包括心脏瓣膜狭窄在内的非典型类早衰特征。
在家族2中发现的变体位于家族1中发现的变体附近,也在外显子2中。虽然这种变化在文献中也没有具体描述,但描述HGPS患者的首批研究之一也注意到了一个具有从头变异的病例,该变异导致了不同的氨基酸变化,但位置与家族2中发现的位置(p.Glu145Gly)相同(p.Glu145Lys: rs60310264,在GnomAD v4.0.0的参考等位基因中不存在)。不幸的是,该患者没有全面的表型。
在当前研究中发现的两种变体都位于1B螺旋区(由UniProtKB确定,条目P02545)的中间丝极畴。1B杆结构域是核纤层蛋白A网络的主要组成部分。这一领域的致病遗传变异被认为会破坏网络组装,导致细胞核变形和脆弱。经典类祖细胞表型的变异常常影响N或C端结构域。异常或截短蛋白的形成通常但不总是导致C端残基的法尼基化。这产生了一种高度稳定的前核纤层蛋白,也称为“类核纤层蛋白”。这种蛋白质对细胞有毒,并通过多种机制诱导衰老。此外LMNA-基因与各种其他基因相互作用,可能在基因型-表型相关性中发挥作用。例如,LMNA与基因相互作用,包含核包膜的血影蛋白重复序列(1/2和Emerin(EMD)与EDMD有关联。LMNA也与锌金属肽酶STE24(ZMPSTE24)吉恩。的突变ZMPSTE2在人类中导致各种类祖细胞表型。除了其他遗传因素的潜在作用外,已提出多种机制在不同临床衰老表型的发展中发挥作用,包括表观遗传学、应激反应、炎症和机械信号传导。不幸的是,没有功能性分析来研究患者的蛋白质产物或受影响的途径或特定的遗传变异。因此,不能排除影响患者特定表型的其他遗传或环境修饰因素的潜在作用。
而LMNA在目前的研究中发现的基因变异以前没有被描述过,许多其他的LMNA据报道,基因变异与非典型早衰症表型相关,其严重程度低于典型的HGPS综合征或沃纳综合征,并可能对不同组织产生不同影响。例如,一个有趣的变异是p.Asp300Asn的变化,该变化已在一名29岁女性的急性心肌梗死患者中得到描述。在10年的时间里,在没有传统心血管风险因素的情况下,她出现了广泛的冠状动脉疾病、瓣膜疾病(需要进行置换手术)和心律失常。在一个日本家族中也描述了这种相同的变异体,该家族具有影响血管、皮肤和骨骼等的非典型类骨质疏松症特征。
最近的研究讨论了核纤层蛋白在不同细胞类型中的潜在差异作用以及核纤层在心脏应激反应中的重要性。
本病例系列描述了两个具有看似“孤立”的心脏前体细胞特征的家族和两个先前未描述的家族LMNA-外显子2中的基因错义变体。这些的隔离LMNA-具有该表型的基因变体在这些家族中起致病作用。目前的结果强调了椎板病变的异质性。这些新的见解强调了心脏病专家意识到一种可能的LMNA-基因变异是主动脉瓣和二尖瓣过早狭窄的潜在原因。对于被诊断患有这些疾病的患者LMNA-基因变异,应建议对家族进行心脏筛查,以密切监测并及时识别和治疗瓣膜疾病。然而,未来的研究需要了解这些变异如何导致这些主要影响主动脉瓣和二尖瓣的非典型前体特征。
医博士编译自:Wu HW, Van de Peppel IP, Rutten JW, et al. Atypical Progeria Primarily Manifesting as Premature Cardiac Valvular Disease Segregates with LMNA-Gene Variants. Journal Of Cardiovascular Development And Disease. 2024; 11(3):86. doi:10.3390/jcdd11030086.
声明: 所有注明“来源:医博士”的文字、图片和音视频资料,版权均属于医博士所有,转载须注明“来源:医博士”;所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。