良性肾上腺皮质腺瘤转化为转移性肾上腺皮质癌
来源:医博士 | 2024-11-01
腹部横断面成像中发现的肾上腺肿瘤发病率在5%-7%之间,并且随着年龄的增长而增加。在过去的20年里,肾上腺肿瘤的发病率增加了10倍,与此同时,腹部计算机断层扫描(CT)和磁共振成像(MRI)研究也在增加。作为肾上腺偶发瘤(AI)的肾上腺皮质腺瘤(ACA)恶化为肾上腺皮质癌(ACC)极为罕见,发病率低于1%。然而,这一数字因ACA的大小而异,4-6cm的恶变率为2%,>6厘米的恶变率为25%。
最近的指南建议,所有AI最初都应该用非增强CT进行评估,以估计其脂质含量以及外观是否均匀。如果非增强CT与基线密度<10 Hounsfield(HU)的良性肾上腺肿块一致,则不建议进一步成像。尽管这种方法具有成本效益,并减轻了定期调查的负担以及辐射暴露的危险,但已有最初诊断为ACA的罕见ACC病例。
本文报告了一名64岁男性患者的病例,该患者被诊断为非功能性ACA,在初步诊断13年后恶化为ACC。
病例介绍
2010年,一名有高血压病史的64岁男性吸烟者因腹部不适进行腹部CT检查后,被偶然诊断出左肾上腺有3厘米的同质病变。病变密度<10HU,因此倾向于ACA。激素检查显示没有激素分泌过多的证据。患者在前3年每年接受腹部CT,然后每2年随访一次。病变的大小和影像学特征一直保持稳定,直到2017年失访。
2021年进行的CT扫描显示,病变稳定,为3cm,但非增强衰减值较高,为24HU(图1)。激素筛查显示没有激素分泌过多。2年后,患者在3个月内体重明显减轻,伴有疲劳和腹痛。腹部CT显示,左侧肾上腺存在12×11.5×8.6 cm的异质性病变,表现为周围结构弥漫性浸润(图2)。
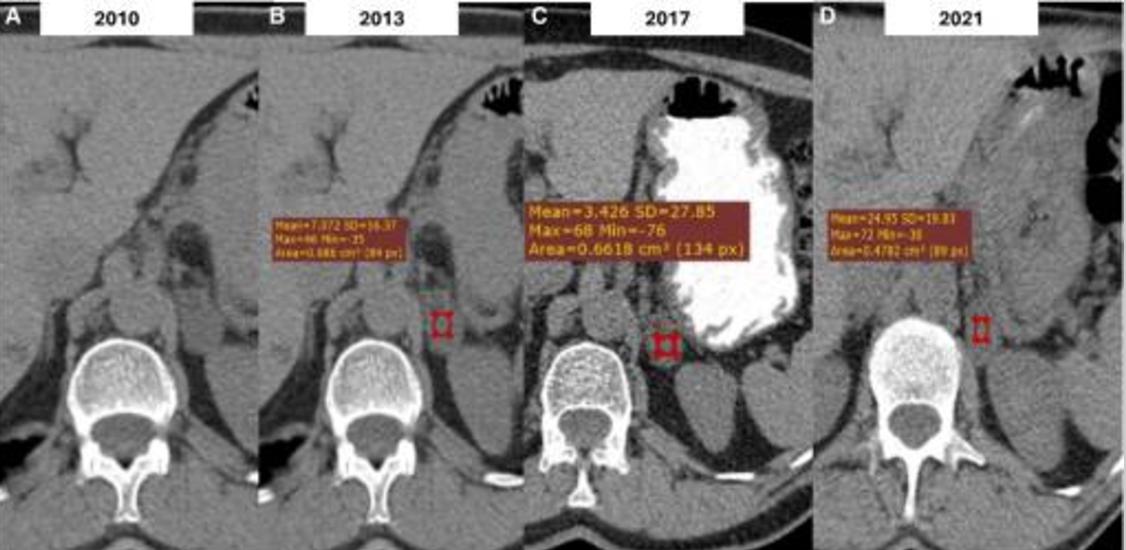
图1 上腹部轴向非增强计算机断层扫描(CT)图像显示,左侧肾上腺结节状病变大小为3cm,低衰减值<10HU,与腺瘤一致(a)。同一患者的随访CT图像显示,病变的大小或密度没有显著变化,平均值±标准差密度值等于7±16.37 HU(最大=46,最小=-35)(B)和3.4±27.85 HU(最大=68,最小=-76)(C)。在肾上腺皮质癌(ACC)诊断前一年进行的随访CT中,病变的大小保持稳定,但显示出较高的平均值±标准差密度值,等于24±19.83 HU(D)
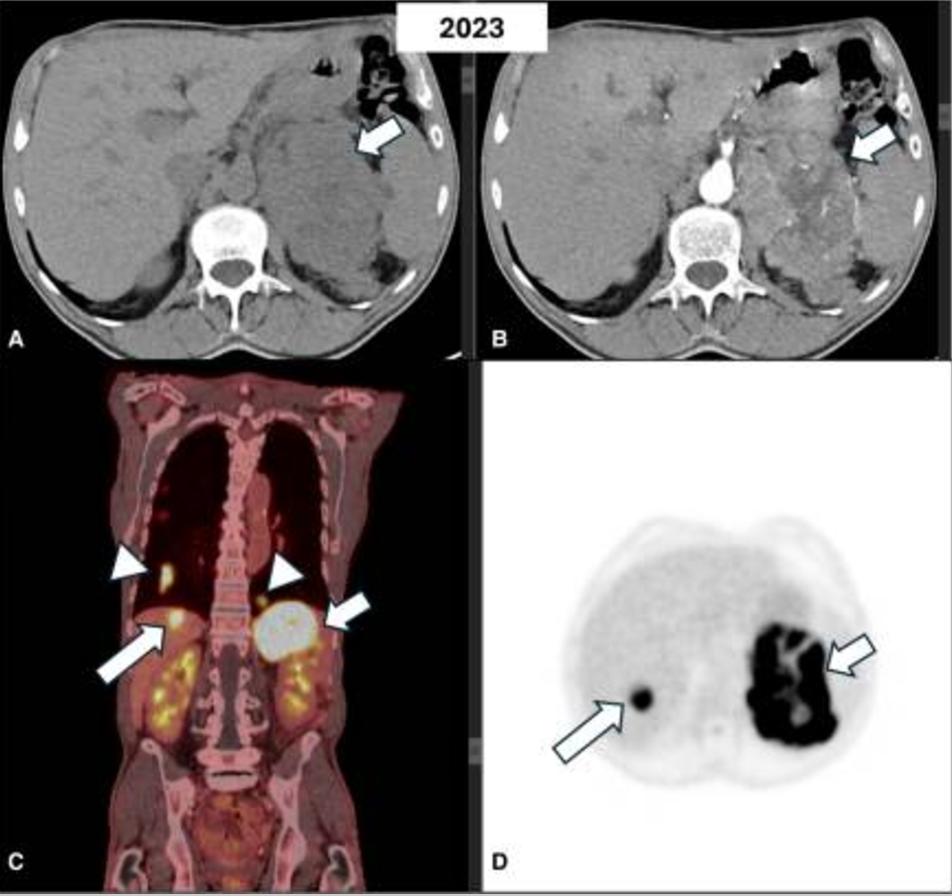
图2 同一患者在静脉注射造影剂之前(A)和之后(B)的腹部轴位计算机断层扫描显示,存在一个异质性肿块,中心坏死灶累及左肾上腺并延伸到周围组织(箭头)。在18FDG-PET图像(C-D)上,病变显示18FDG摄取旺盛(小箭头),肝脏(长箭头)和肺部(箭头)出现高代谢活性病变,怀疑有转移
MRI证实存在增大的不均匀左肾上腺肿块,并伴有强烈的对比增强(图3A-3C)。此外,肝脏中描述了2个新的可疑病变,其中1个在第VIII段为2cm,另一个在第VI段为7.7mm,倾向于转移性疾病(图3A-3C)。胸部CT还显示了多个继发性双侧肺部病变(图4A)。18FDG-PET显示,肾上腺病变(18SUVmax)、肝和肺病变(10-12SUVmax)和左肾上腺静脉(12SUVmix)的摄取增加,与血管血栓一致(图2)。
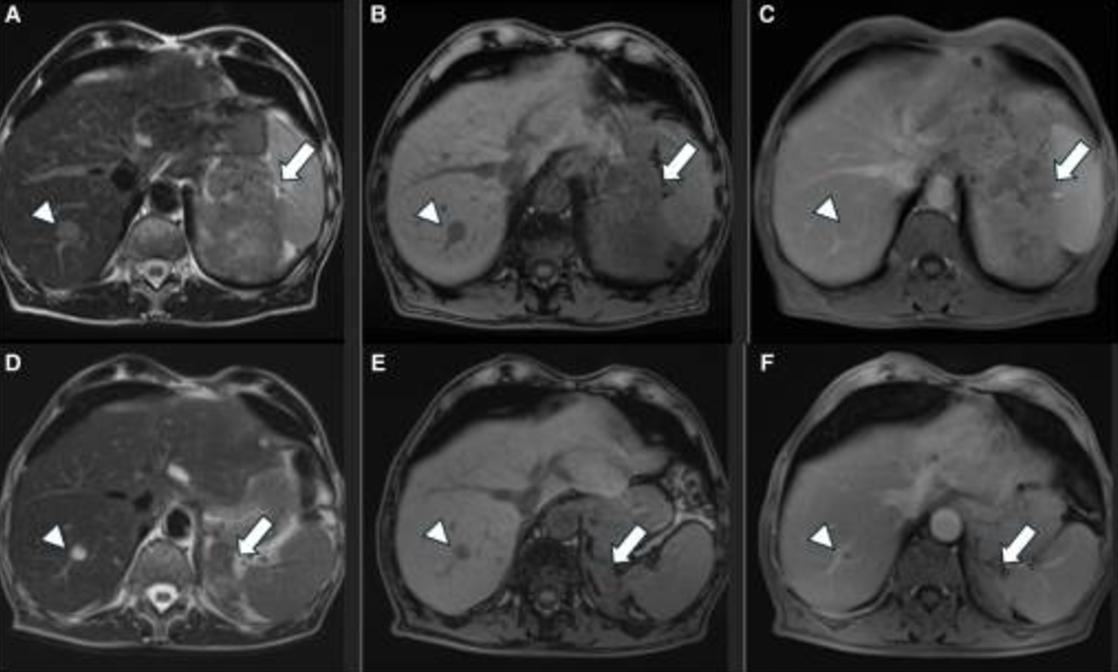
图3 同一患者治疗前和治疗后6个月的MRI。治疗前轴向T2W STIR(A)、T1反相(B)和对比增强T1W SPIR(C)图像显示,左侧肾上腺存在异质性肿块(A和B中的箭头),并具有强烈的对比增强(C中的箭头。右肝叶也可见肝转移(A-C中的箭头)。相应的治疗后MRI显示肾上腺病变大小显著减小(D-F中的箭头)。注意对比后图像上病变的最小增强(F中的箭头),这是肿瘤对治疗反应的另一个发现。在治疗后MRI上,肝脏病变也减少(D和E中的箭头),增强程度较低(F中的箭头)
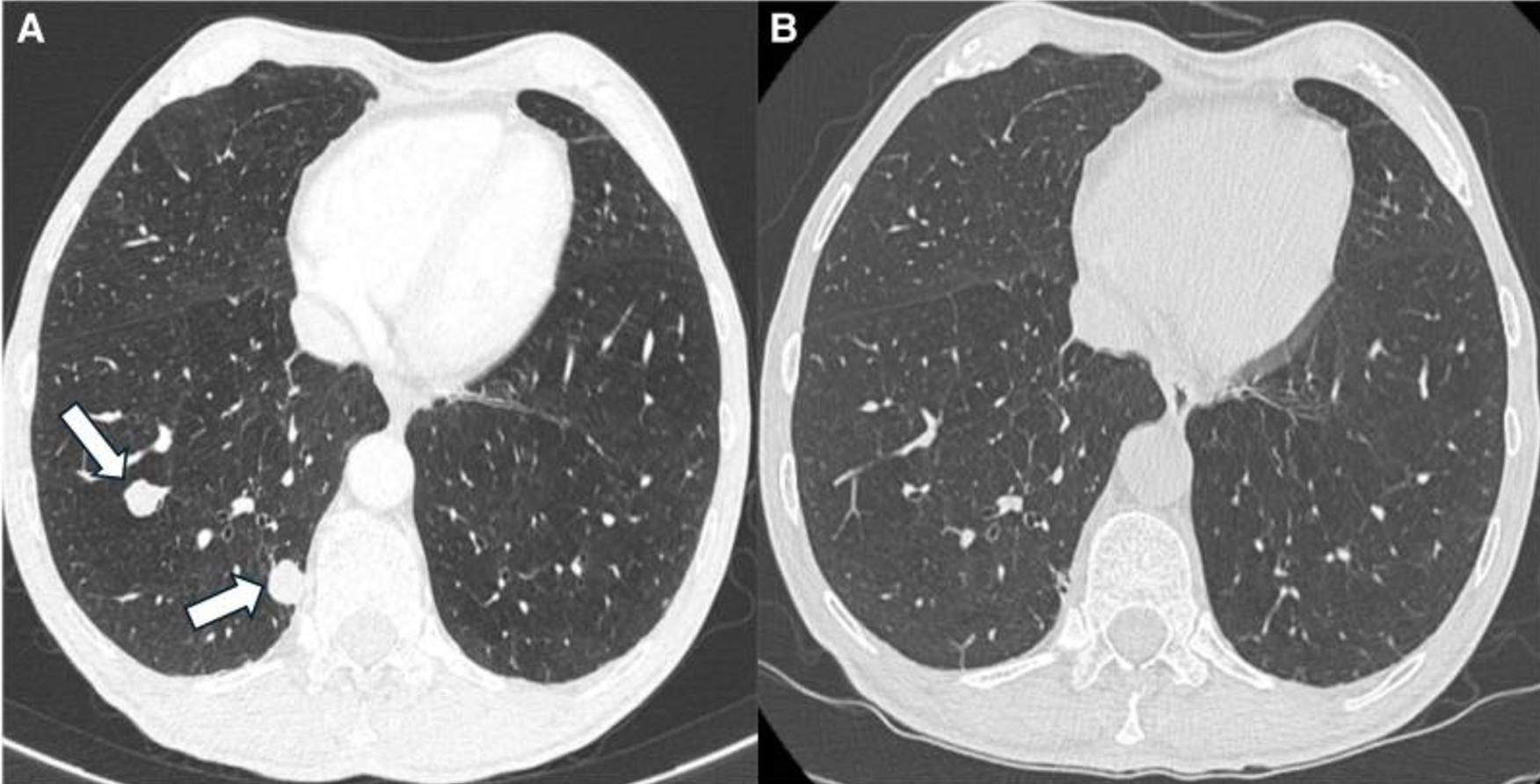
图4 患者治疗前后肺部CT。初始表现(A)的轴位CT图像显示右下叶有2个边界清晰的肺结节(箭头),与转移一致。治疗6个月后,相同水平(B)的相应CT图像显示转移结节完全消退
临床上,患者表现为恶病质但血压正常,没有任何库欣综合征的迹象。激素谱显示皮质醇和雄激素分泌过多。对1个肝脏病变的活检证实了Ki-67标记指数(LI)为70%的高级别ACC转移。免疫组织化学分析显示类固醇生成因子1、突触素+和黑色素A+呈阳性,泛角蛋白、上皮膜抗原和嗜铬粒蛋白A呈阴性。基于肝转移转录组分析的分子分类使用福尔马林固定石蜡包埋样品进行3′RNA测序,该样本被归类为“C1A”,预示着不良结果(图5)。
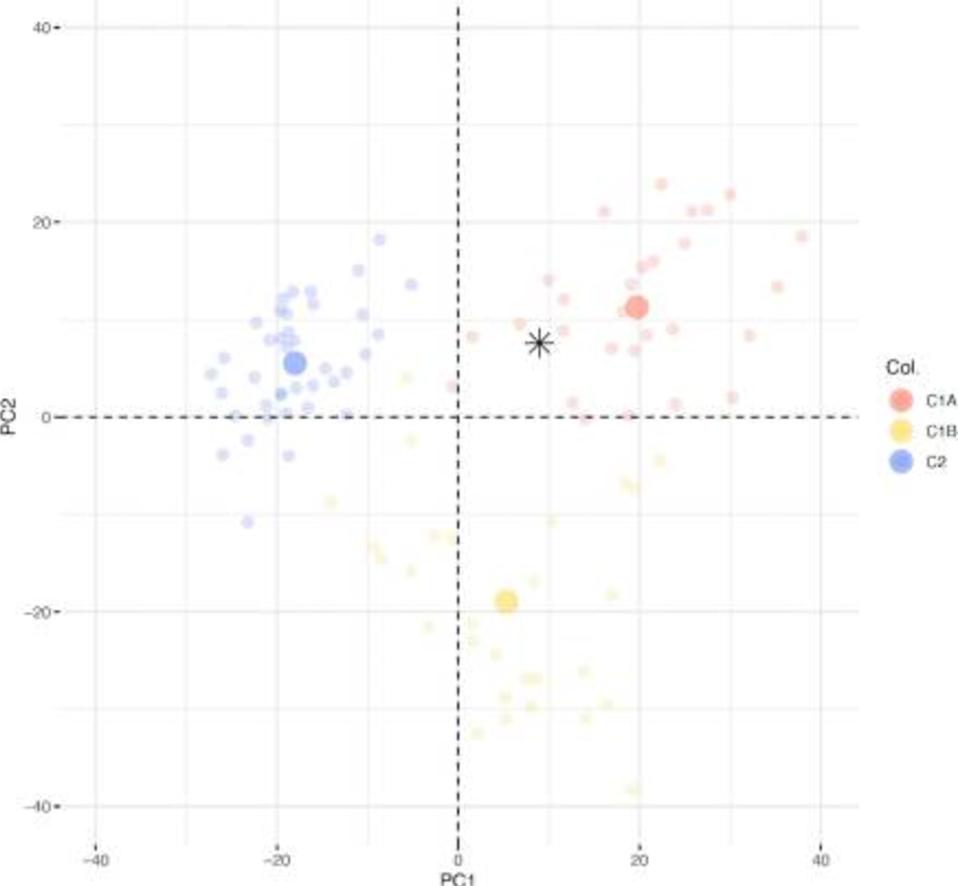
图5 转录组分类。在95名患者的参考队列中,将患者样本(*)投影到主成分分析(PCA)的两个主成分(Dim1、Dim2)上。来自该参考队列的样本以转录组类别着色的淡圆圈表示:蓝色表示肾上腺皮质腺瘤“C2”,红色表示预后不良的肾上腺皮质癌“C1A”,黄色表示预后较好的肾上腺皮质癌“C1B”
该病例进行多学科会诊,不建议手术治疗。患者开始接受高剂量米托坦(最多6克)治疗,在8周内达到22.5毫克/升的水平,因为有明显的副作用,将米托坦剂量滴定到每天4.5克。还需要用氢化可的松和氟氢可的松进行替代治疗。根据FIRMACT研究,患者同时接受了6个周期的化疗(依托泊苷、阿霉素和顺铂)。
在开始米托坦和化疗治疗2-3周后,出现了3级副作用,包括恶心、疲劳、不稳定、神经传感器症状以及记忆和注意力困难。此外,患者出现骨质疏松性右colles骨折,需要服用地诺单抗。
两种治疗后3个月的成像显示,所有病变都有部分反应,6个月时,根据RECIST 1.1标准,肾上腺和肝脏病变有进一步的部分反应(图3D-3F),肺转移完全消失(图4B)。患者在ACC诊断后8个月仍然活着,仅继续接受米托坦治疗。
小结
ACC是一种罕见的疾病,起源于ACA的ACC更为罕见,但确实存在。根据最近的指南,对具有良性成像特征的AI成像随访进行了修改,以避免过度检查。考虑到持续监测和不必要的辐射暴露对识别可能有患ACC风险的患者的潜在影响,需要开发额外的预测性生物标志物来潜在地识别可能表现出这种过程的患者。
医博士编译自: Angelousi A, Jouinot A, Bourgioti C, et al. Transformation of a Benign Adrenocortical Adenoma to a Metastatic Adrenocortical Carcinoma Is Rare But It Happens. JCEM Case Reports. 2024;2(8):luae131. doi:10.1210/jcemcr/luae131.
声明: 所有注明“来源:医博士”的文字、图片和音视频资料,版权均属于医博士所有,转载须注明“来源:医博士”;所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。