极为罕见:癌症腋窝脂肪转移
来源:医博士 | 2025-10-15
乳腺癌是世界范围内最常见的恶性肿瘤之一,也是癌症相关死亡率的第二大原因。2022年,约230万女性被诊断出患有乳腺癌,导致约67万人死亡。
转移是90%以上乳腺癌相关死亡的原因,其中腋窝淋巴结是最常见的转移部位。在晚期,癌症通常转移到肺、骨、肝和脑等器官。这些转移模式是由肿瘤细胞的内在特性和靶器官独特微环境之间的复杂相互作用决定的。关键机制包括:i)趋化因子受体相互作用,如骨转移中的C-X-C基序趋化因子(CXC)配体12-CXC受体4轴;ii)将循环肿瘤细胞引导到具有丰富毛细血管网络的器官的血流动力学因素;iii)富含生长因子和细胞外基质成分的支持性微环境。相比之下,脂肪组织对转移具有多种生物屏障,包括稀疏的血管化、关键粘附分子的缺失以及以缺氧和酸中毒为特征的代谢不良环境。这些障碍使其成为肿瘤细胞定植和增殖的不利环境。在晚期疾病和广泛的血行扩散的患者中,偶尔会观察到癌症转移到脂肪组织,通常伴有转移到其他器官。孤立性脂肪组织转移极为罕见。
病例介绍
2024年11月,一名54岁的女性住院治疗,患者在入院前6个月内注意到左乳房有一个肿块,但由于没有疼痛、皮肤刺激或乳头溢液等症状而延迟就医。入院时,主治医生进行的全面体检显示,左乳房上外象限有一个直径约2厘米的坚硬、活动性差的肿块。肿块与周围组织轻度粘连。腋窝或锁骨上区域未发现明显的淋巴结病。此外,心血管、呼吸和腹部系统的常规体检未发现异常。患者无特殊既往病史。
乳房X线摄影显示,左乳房上外象限有一个高密度、不规则形状的肿块,大小约为35×24 mm,边缘呈毛刺状,内部钙化(图1A)。此外,乳腺MRI显示左乳腺上外象限有一个约20×18mm的肿块,形状不规则,边缘呈毛刺状。T1加权图像显示病变信号强度低,脂肪饱和T2加权图像显示混合信号,对比增强图像显示显著增强(图1B和C)。此外,彩色多普勒乳腺超声显示,在左乳房2-3点钟位置距离乳头4厘米处有一个低回声结节,尺寸约为20×14毫米(图1D)。注射造影剂后,病变大小为35×17 mm,表现出不均匀的高增强和突出的血管结构(图1E)。穿刺活组织检查显示左乳房存在侵袭性乳腺癌症(图S1A和B)。免疫组织化学(IHC)结果显示,活检样本细胞Ki-67呈阳性(30%)(超过14%阈值),雌激素受体(ER)呈强阳性(90%),孕激素受体(PR)呈中度至强阳性(30%),人表皮生长因子受体2(HER2)呈阴性(1+)(图S1C-F)。其他术前检查,包括胸部和腹部计算机断层扫描(CT)、颅脑CT和全身骨扫描,均未发现远处转移或异常的证据。血清肿瘤标志物水平也被评估并证明在正常范围内:癌胚抗原(CEA)为2.64 ng/ml(参考值,<4.7 ng/ml),癌症抗原15-3(CA15-3)为18.9 U/ml(参考值<26.2 U/ml)。最初诊断为左侧乳腺癌(管腔B型,cT2N0M0,IIA期)。肿瘤直径>2cm,没有临床明显的腋窝淋巴结受累,也没有远处转移的迹象,与IIA(cT2N0M0)的临床分期一致。根据这些发现以及免疫组织化学分析的结果,肿瘤被归类为管腔B分子亚型。
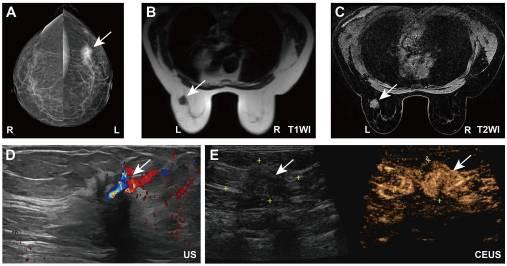
图1 患者的术前影像学数据。(A)乳房X线摄影。(B)T1和(C)T2加权乳腺磁共振成像。(D)彩色多普勒超声和(E)手术治疗前患者的乳腺超声造影。白色箭头表示肿瘤的位置。CEUS,超声造影
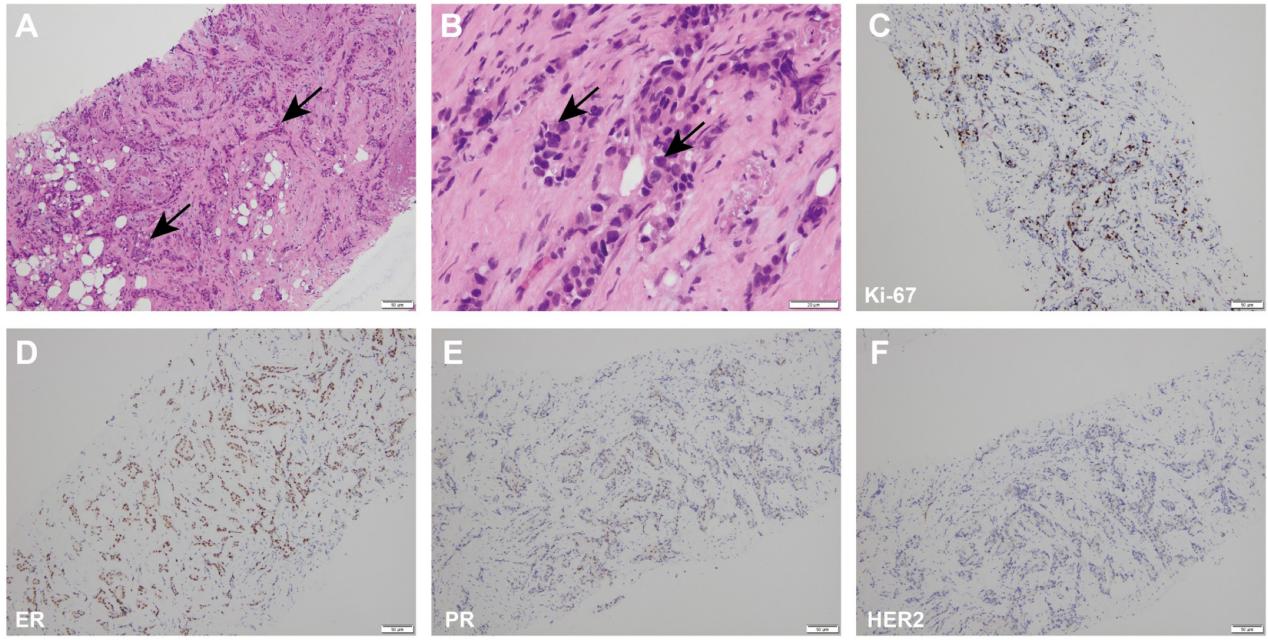
图S1。左乳房穿刺活检标本的病理检查结果。H&E染色,放大倍数为(A)x100(比例尺,50μm)和(B)x400(比例尺,20μm)。黑色箭头表示肿瘤细胞。左乳腺穿刺活检标本中的IHC(C)Ki-67(放大倍数,x400;比例尺,50μm)、(D)ER(放大倍率,x400,比例尺,50微米)、(E)PR(放大倍数,x400;比例尺,50μm)、(F)HER2(放大倍数,x400;比例尺,50μm)。免疫组织化学;ER,雌激素受体;PR,孕激素受体;HER2,人表皮生长因子受体2
2024年12月,患者在全身麻醉下接受了左腋窝前哨淋巴结活检和左乳房象限切除术。手术过程中,切除前哨淋巴结和邻近脂肪组织,并送去进行术中病理分析。对冷冻切片的分析确定了四个来自左腋窝的前哨淋巴结,所有这些淋巴结都是无癌的。随后切除左乳房肿块并进行冷冻切片分析。使用低温恒温器快速冷冻标本,切片厚度为5-10µm,用苏木精和伊红(H&E)染色,并立即由病理学家在光学显微镜下进行评估。分析证实了侵袭性癌症。肿瘤边缘由内、外、上、下、基底和皮瓣组成,被确定为无癌。手术顺利完成,无并发症,患者顺利康复。切除的乳腺组织的术后病理分析证实了侵袭性乳腺癌症(图2A和B)。
根据诺丁汉组织学评分系统对乳腺肿瘤进行组织学分级,该系统评估了三个形态特征:小管形成、核多形性和有丝分裂计数。每个组成部分的评分为1-3分,总分按如下方式确定等级:I/G1级(分化良好;评分3-5分),其中肿瘤与正常乳腺组织非常相似,增殖性较低,通常表明预后良好;II/G2级(中度分化;评分6-7),其中肿瘤表现出中等分化水平和预后;III/G3级(低分化;评分8-9),其中肿瘤表现出明显的异型性、高有丝分裂活性和侵袭性临床行为,预后较差。癌症病灶分为诺丁汉Ⅱ级/G2级(总分6分)。
术后病理检查证实,根据切除标本的大体检查,肿瘤大小为35×26×15mm。组织学分析进一步证明了神经侵袭的存在(图S2A)。血管内皮细胞的特异性标志物CD34的IHC染色为阴性,进一步证实没有淋巴或血管浸润(图S2B)。此外,所有手术切缘,包括12、3、6和9点钟方向以及深(基底)和浅(皮肤)切缘,均未发现肿瘤受累(图S2C-H)。IHC结果表明,切除的左乳腺组织中的细胞Ki-67呈阳性(热点约30%),ER呈强阳性(90%),PR呈中度阳性(30%),HER2呈阴性(1+)(图2C-F)。此外,左腋窝前哨淋巴结的病理检查显示,有四个淋巴结没有转移的迹象。然而,在其中一个淋巴结附近的脂肪组织中检测到浸润性导管癌(图3A和S3)。腋窝前哨淋巴结和脂肪组织的IHC分析显示,脂肪组织中泛细胞角蛋白呈阳性染色,而淋巴结中没有观察到表达(图3B)。这一发现证实了肿瘤侵入腋窝脂肪组织,而不是淋巴结。肿瘤病灶被归类为诺丁汉I/G1级(总分5),大小约为3.3×1.9 mm。IHC显示,脂肪组织细胞Ki-67阳性(5%),ER强阳性(90%),PR中度阳性(30%),HER2阴性(1+)(图3C-F)。
基于所有上述发现,患者的术后诊断为左乳腺恶性肿瘤(乳腺癌症,腔B型,pT2N0Mx,IIA期)和左腋窝脂肪组织的继发性恶性肿瘤(腔a型)。
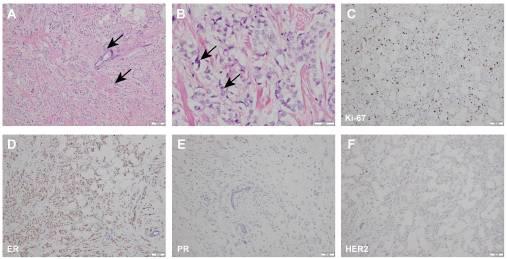
图2 左乳腺肿块切除标本的病理检查结果。放大倍数为(A)×100(比例尺,50µm)和(B)×400(比例尺,20µm)的H&E染色。黑色箭头表示肿瘤细胞。左乳腺肿块切除标本中的IHC(C)Ki-67(放大倍数,×100;比例尺,50µm)、(D)ER(放大倍率,×100,比例尺,50μm)、(E) PR放大倍率,×100,比例尺,50μm)、(F)HER2(放大倍率,×100,比例尺,50μm)。ER,雌激素受体;PR,孕激素受体;HER2,人表皮生长因子受体2
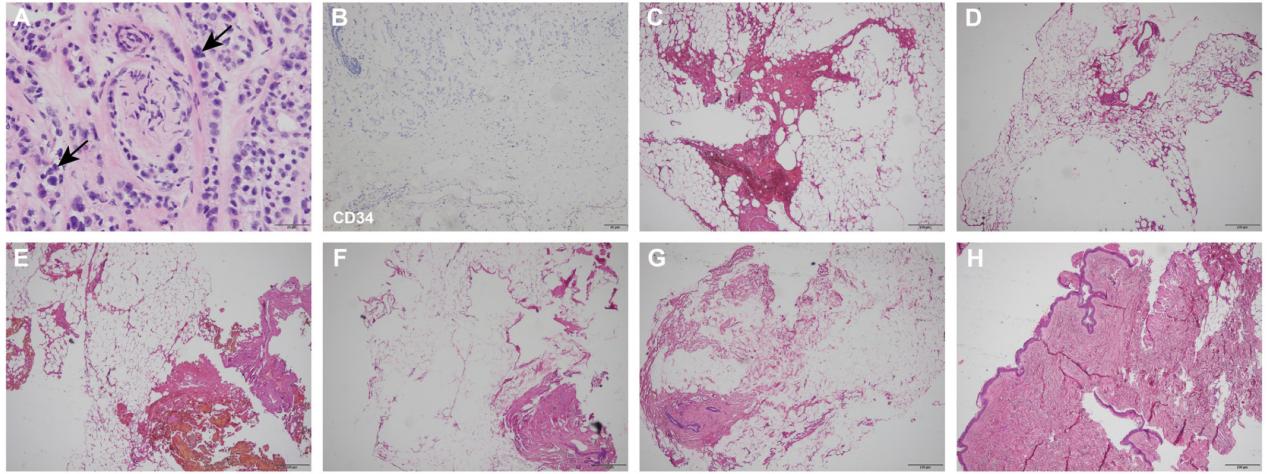
图S2 术后乳腺组织的组织学发现。(A)H&E染色显示肿瘤细胞对神经的侵袭(黑色箭头;放大倍数x400;比例尺20μm)。(B)CD34的IHC显示肿瘤微环境中没有淋巴血管浸润的证据(放大倍数,x400;比例尺,50μm)。H&E染色显示在多个方向确认的阴性手术切缘:(C)12点钟,(D)3点钟,(E)6点钟,(F)9点钟,(G)基底(深)和(H)浅(皮肤),在任何切缘都没有观察到残留的肿瘤细胞(放大倍数,x20;比例尺,200μm)
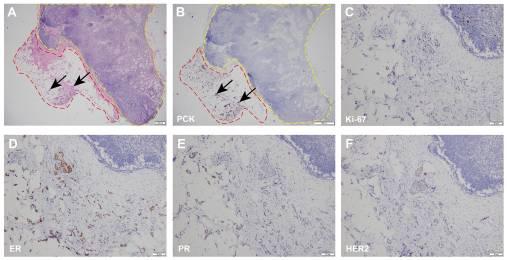
图3 左腋窝前哨淋巴结和脂肪组织的病理检查结果。(A)放大20倍的H&E染色(比例尺,200µm)。左腋窝前哨淋巴结和脂肪组织中的(B)PCK(放大倍数,×40;比例尺,200µm)、(C)Ki-67(放大倍数:×100;比例尺,50µm),(D)ER(放大倍数:×100;比例尺,50µm)、(E)PR(放大倍数:×100;比例尺,50µm)和(F)HER2(放大倍率:×100,比例尺,50μm)。黄色虚线框表示左腋窝前哨淋巴结,红色虚线框表示与左腋窝前哨淋巴细胞相邻的脂肪组织(转移性病变)。黑色箭头表示肿瘤细胞。PCK,细胞角蛋白;ER,雌激素受体;PR,孕激素受体;HER2,人表皮生长因子受体2
患者接受了术后四个周期的化疗,使用多烯紫杉醇+环磷酰胺方案,然后进行乳腺放疗和芳香化酶抑制剂(AI)辅助治疗。目前,患者已完成术后辅助化疗(75 mg/m2多西他赛+600 mg/m2环磷酰胺,每21天为一个周期,2024年12月至2025年3月共四个周期)。在化疗期间,患者出现了白细胞减少症,在药物干预后有所改善。未观察到其他明显的不良事件。2025年4月至5月,进行了保乳术后放射治疗,放射治疗期间,患者左乳房和腋窝出现轻度红斑和肿胀,经局部烧伤软膏治疗后消退。在2025年3月完成化疗后,患者开始接受来曲唑(每天2.5mg)的辅助内分泌治疗,迄今为止没有任何明显的不良反应。
截至2025年5月,随访评估,包括胸部CT、乳房和腹部超声检查以及血清肿瘤标志物评估,均未发现复发或转移的证据。最近的肿瘤标志物水平在正常范围内:CEA为3.05 ng/ml(参考值,<4.7 ng/ml);CA15-3为19.6U/ml(参考值<26.2U/ml)。2025年5月的放射学随访成像也没有发现异常:胸部CT显示没有肺或纵隔转移的证据(图4A),乳房超声检查显示左乳房术后变化,没有局部复发的迹象(图4B),腹部超声检查没有发现肝或腹膜病变(图4C)。此外,根据2024 CSCO乳腺癌症指南,建议患者继续接受基于AI的内分泌治疗5年,以及随访监测计划,包括每3个月进行一次乳腺超声检查,每6个月进行乳腺MRI和肿瘤标志物评估。
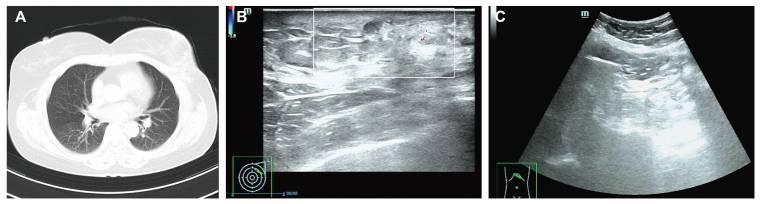
图4 患者的放射学随访成像。(A)胸部计算机断层扫描显示没有肺或纵隔转移的证据。(B)乳房超声检查显示左乳房术后变化,无局部复发迹象。(C)腹部超声检查显示无肝脏或腹膜异常
小结
同侧腋窝淋巴结被广泛认为是癌症上外象限最常见的转移部位。尽管腋窝脂肪组织在解剖学上与乳房相邻,但癌症完全转移到腋窝脂肪组织而不涉及前哨淋巴结或其他常见转移部位的情况极为罕见。提高对脂肪转移的临床认识至关重要,特别是在传统转移途径不能完全解释临床表现的情况下。
医博士编译自:Zhang S, Chen J, Zhang Y, et al. Axillary fat metastasis in breast cancer: A case report. Oncology Letters. 2025; 30(3):412. doi:10.3892/ol.2025.15158.
声明: 所有注明“来源:医博士”的文字、图片和音视频资料,版权均属于医博士所有,转载须注明“来源:医博士”;所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。