地诺单抗致外耳道骨坏死2例
来源:医博士 | 2025-11-24
药物相关性颌骨坏死是一种罕见但公认的抑制骨吸收药物治疗并发症,药物相关性外耳道骨坏死更为罕见,主要在双膦酸盐暴露期间报告。
双膦酸盐和地诺单抗是常用于治疗骨质疏松症、骨转移和其他骨骼疾病的药物。人们普遍认识到这些药物会增加药物相关性颌骨坏死(MRONJ)的风险。在开始使用抗骨吸收剂治疗前,建议进行常规牙科筛查,并有关于管理MRONJ高危患者的指南。然而,一种类似但更罕见的并发症是药物相关性外耳道坏死(MROEAC),迄今为止,已有30多例相关病例报告,其中大多数与双膦酸盐有关。这种鲜为人知的并发症可能表现为耳痛、耳漏、听力丧失或面神经功能障碍,偶尔无症状被偶然发现。本文描述了两例与地诺单抗使用相关的无诱因MROEAC病例,以强调在停用地诺单抗后出现严重骨缺失时后续治疗的复杂性。
案例A
一位72岁女性患者,主诉左耳瘙痒逐渐加重5年,无耳痛、耳漏或耳道外伤史。2018年,
为治疗骨质疏松症以及既往桡骨和跖骨脆性骨折,患者开始每6个月注射一次60mg地诺单抗(持续5年)。既往病史包括稳定的不明原因单克隆丙种球蛋白病(MGUS)(免疫球蛋白M kappa 15克/升),伴有轻度免疫球蛋白G抑制(5.43,参考范围:6.1-16.2克/升)、双侧对称性高频感音神经性听力损失(无需助听器)、慢性阻塞性肺疾病、胃食管反流(每日服用20毫克泮托拉唑控制)以及10年前的肾结石。患者未接受过全身性糖皮质激素治疗。
2023年5月,一位耳鼻喉科医生通过耳镜检查发现,患者左外耳道底有侵蚀和骨外露。计算机断层扫描(CT)成像证实了骨侵蚀和软组织改变,支持该诊断(图1)。侵蚀采用保守治疗,每次耳鼻喉科复查时滴入复方康纳乐霜(曲安奈德0.1%+新霉素0.25%+短杆菌肽0.025%+制霉菌素100,000单位/克)。临床诊断为多发性复发性外耳道脓肿(MROEAC),认为是由地诺单抗所致。
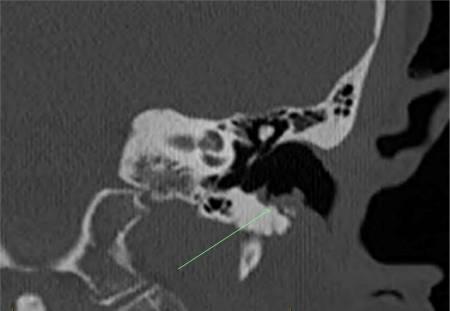
图1 病例A—左耳道冠状位CT扫描,箭头显示下耳道侵蚀区域,上覆分叶状软组织
根据外耳道骨坏死的诊断,2023年6月停止使用最后一剂地诺单抗,并于当月开始每天皮下注射20mcg特立帕肽。患者出现了短暂的高钙血症,校正钙为2.75mmol/L(参考范围:2.10-2.60 mmol/L),当时没有服用钙补充剂。此外,2023年11月,出现了多发性症状性双侧草酸钙肾结石,需要支架治疗。由于患者担心高钙血症和肾结石,2023年12月停用特立帕肽。患者不愿意继续以当前剂量或降低剂量频率服用特立帕肽。
在停止特立帕肽治疗时发现,尿钙排泄量低至2.0 mmol/d(参考范围:2.5-7.5 mmol/d),尿草酸排泄正常,1型胶原C末端肽(CTx)升高至1110 ng/L(参考范围为100-1000 ng/L),1型前胶原氨基末端肽(P1NP)升高至132μg/L(参考范围15-115μg/L)。她当时的DXA扫描(Hologic)显示,左侧FN的T评分为-1.6,腰椎为-2.2,桡骨远端为-0.9。与2018年在不同的分析仪上进行DXA(Lunar)相比,FN和LS的基线T评分分别为-1.6和-1.9。骨盆、双侧股骨和胸腰椎的X光片上没有发现骨折,而停止使用地诺单抗和特立帕肽后,左耳道的暴露骨面积没有变化(图2A)。右耳道正常(图2C)。
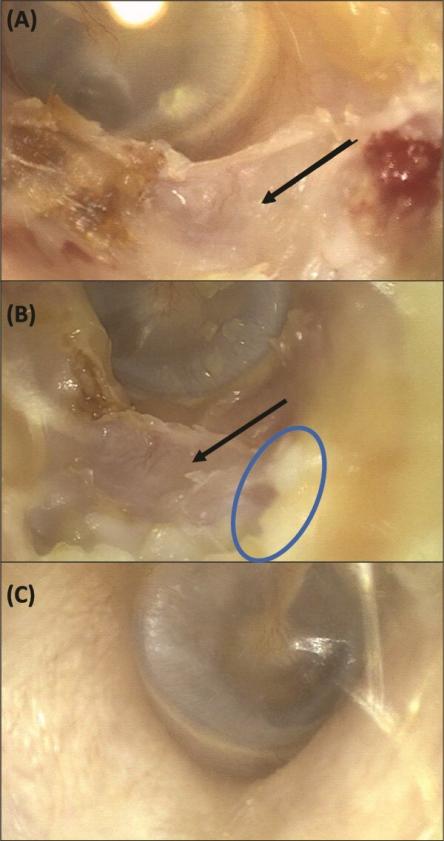
图2 病例A的耳镜图像。(A)利塞膦酸钠治疗后1个月的左外耳道:鼓膜位于内侧,有皮肤缺损,外耳道骨暴露在下方(黑色箭头)。(B)利塞膦酸钠治疗后7个月的左外耳道:骨缺损减少(黑色箭头),上方的早期上皮化(蓝色圆圈)。(C)右外耳道正常
告知患者,由于不同DXA制造商提供的图像,对骨缺失趋势的解释有限。患者于2024年2月开始服用利塞膦酸钠,并定期于耳鼻喉科进行耳道清洗和涂抹复方康纳乐霜。利塞膦酸钠耐受良好,无胃食管反流症状,开始6个月后进行的血液检查显示,骨转换标志物下降(表1),耳镜检查发现早期愈合和上皮化(图2B)。在2025年6月的最后一次检查发现皮肤再生持续改善,只有一小部分暴露的骨质。
案例B
一名84岁的男子因2年的左耳不适和瘙痒病史就诊耳鼻喉科。2018年开始每6个月注射60毫克地诺单抗用于治疗骨质疏松症,无脆性骨折。在2018年LS基线骨密度T评分为-2.7,在2021年(相同的Lunar分析仪)地诺单抗治疗后,这一评分提高到-2.0。耳道之前没有外伤,没有使用棉签,也没有接触过系统性糖皮质激素。既往史包括膝骨性关节炎、血脂异常、空腹血糖受损、缺血性心脏病、维生素B12缺乏症、腹股沟疝和股疝、前列腺肥大以及切除术后治愈的直肠腺癌。耳镜检查显示,左外耳道下段有大量碎片,有小面积骨外露(图3A)。鉴于左侧MROEAC的临床诊断,他接受了局部软膏治疗,并被转至内分泌科。
经过评估,停用地诺单抗(最后一剂2024年5月),密切监测骨转换标志物并每月耳鼻喉科就诊滴入复方康纳乐霜(曲安奈德0.1% + 新霉素0.25% + 短杆菌肽0.025% + 制霉菌素100,000单位/克)。鉴于患者的年龄和偏好,没有进行特立帕肽治疗。2024年1月开始每周服用35 mg利塞膦酸钠,此时CTx升至中标准范围的50%以上(表1),4个月后CTx减少,耳痛缓解,暴露骨减少,早期上皮化(图3B)。右外耳道保持正常(图3C)。
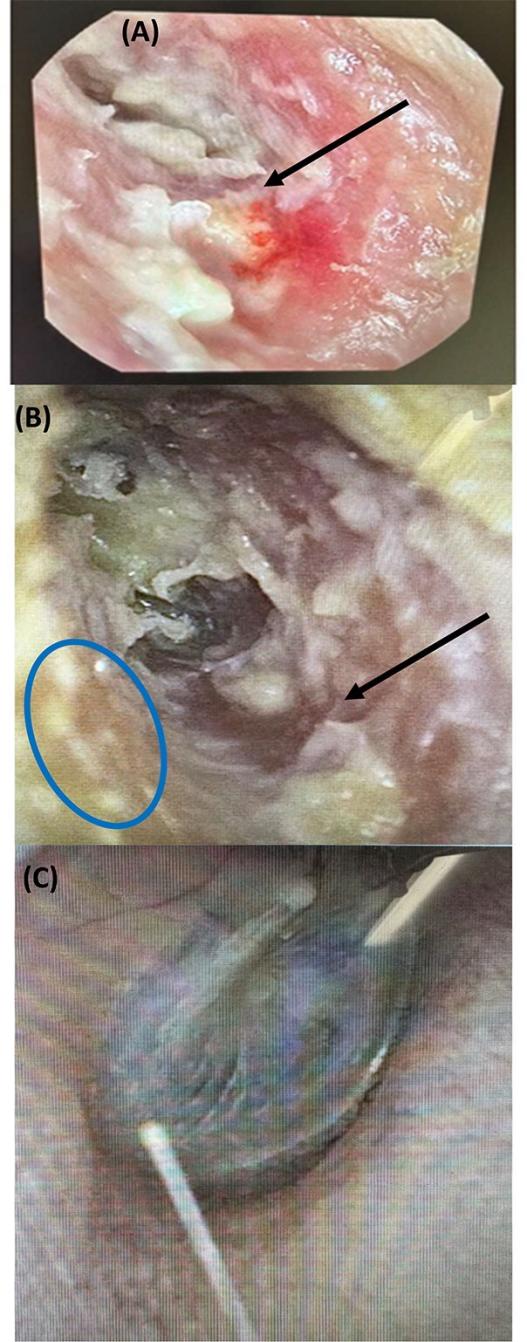
图3 病例B的耳道耳镜图像。(A)单抗治疗时的左外耳道:鼓膜位于内侧,被碎片、皮肤缺损和骨裸露所遮挡(黑色箭头)。(B)利塞膦酸钠治疗后6个月的左外耳道:骨缺损减少(黑色箭头)上方的早期上皮化(蓝色圆圈)。(C)右外耳道正常
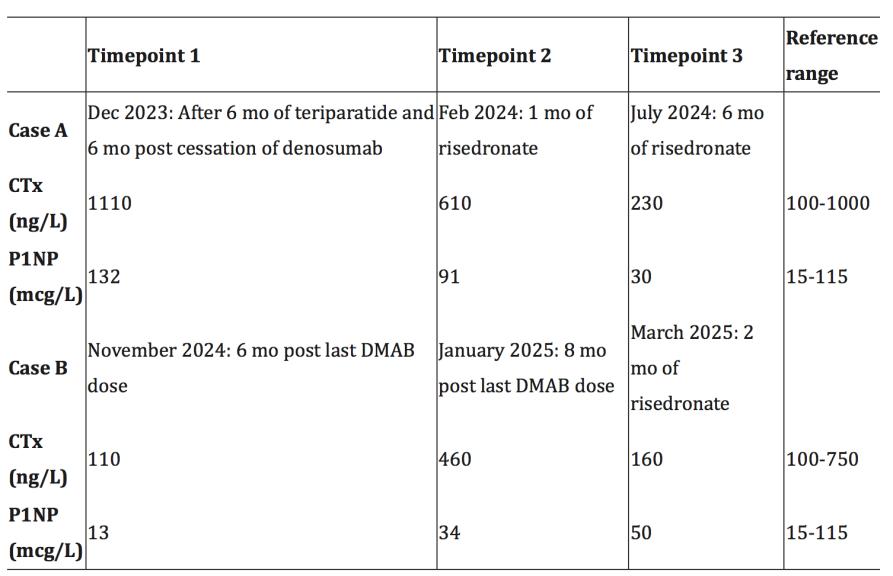
表1 病例A和B的骨转换标志物变化
讨论
药物相关性颌骨坏死是抗骨吸收药物的一种常见并发症。在肿瘤患者群体中,其发病率约为1%-15%,在骨质疏松症患者群体中为0.001%-0.01%,更可能随着累积剂量的暴露而发生。
据报道,双膦酸盐可在拇指和颅骨等意外部位引起骨坏死。影响耳道的双膦酸盐相关骨坏死病例报告可追溯到2007年7月9日,首次在2021年使用地诺单抗的患者中报告。
MRONJ和MROEAC的潜在病理生理学被认为是相似的,涉及多个过程,包括抑制骨重塑、改变血管生成、感染和炎症以及改变免疫功能。感染和炎症被认为是骨坏死过程中的关键组成部分,尽管尚不清楚感染后是否会出现坏死,反之亦然。在牙科感染区域,观察到破骨细胞活动和骨吸收部位的细菌微丝,大多数MRONJ病例是由牙科手术引起的。在有限的MROEAC报告系列中,仅在一例病例中发现了棉签对耳道的损伤。由于创伤并不总是与之相关,MROEAC之前可能会出现外耳道感染和炎症,也称为外耳道炎。外耳炎有明显的危险因素,如耳道狭窄、耳道湿疹、助听器使用者、游泳和潮湿环境。与牙科感染相比,慢性外耳炎的微生物特征也不同,通常伴有真菌和细菌混合感染(如铜绿假单胞菌、金黄色葡萄球菌)。
小结
综上所述,外耳道骨坏死是抑制骨吸收药物的一种罕见且可能未被充分认识的并发症。尽管建议在接受抑制骨吸收治疗前进行牙科检查,但由于需要专业知识,对所有患者进行外耳道评估不太可能具有成本效益。对于已确诊的病例,通常采取支持性治疗,但关于后续骨质疏松症治疗的指南却缺乏。为了管理这些患者,临床医生需要提高认识,并开展进一步研究,以评估停用抑制骨吸收药物以及使用特立帕肽或利塞膦酸钠治疗后,MROEAC的演变情况。
在患者教育中,应权衡抑制骨吸收药物对骨骼的整体益处与MROEAC这一罕见副作用之间的关系。
医博士编译自:Wang H, Yii M, Teh BM, et al. Osteonecrosis of the external auditory canal in two patients on denosumab therapy. JBMR Plus. 2025; 9(10):ziaf134. doi:10.1093/jbmrpl/ziaf134.
声明: 所有注明“来源:医博士”的文字、图片和音视频资料,版权均属于医博士所有,转载须注明“来源:医博士”;所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。