联合使用替罗非班和布洛芬导致的严重血小板减少症:布洛芬是否有关联?
来源:医博士 | 2025-12-30
药物诱导性血小板减少症(DITP)是指由药物暴露引发的血小板计数降低的疾病,于19世纪首次被报道。多数药物通过免疫机制诱发血小板减少症。据统计,成人 DITP 的年发病率约为每百万人口10例。通常,当血小板计数低于 50×10⁹/L 时,患者发生自发性出血的风险会显著升高。本文报道 2 例患者,在短期内出现血小板计数急剧下降的情况,经诊断符合药物诱导性血小板减少症的临床特征。
病例1
患者1为 52 岁男性,既往无特殊病史,因头晕、恶心、头痛、呕吐症状持续 20 余小时入院。头颅磁共振成像(MRI)检查提示:左侧小脑半球及小脑蚓部急性/亚急性脑梗死,颅内多发缺血性梗死灶,右侧大脑中动脉重度狭窄或闭塞。患者入院前因头痛自行服用布洛芬。入院基线血小板计数正常,为 217×10⁹/L。入院后予阿司匹林0.1 g/d、氯吡格雷300 mg/d 口服抗血小板治疗,同时予替罗非班静脉输注,先以0.4 μg/kg/min 的速率输注 30 分钟,随后以0.1 μg/kg/min 的速率维持输注。替罗非班输注37分钟后,患者突发上腹部不适、胸闷、口唇发绀、畏寒症状,测腋温38.8℃,指尖动脉血氧饱和度约90%,血压146/73 mmHg。临床首先考虑急性过敏反应,立即停用替罗非班,并静脉注射地塞米松5 mg。急诊血常规检查提示血小板计数急剧下降至4×10⁹/L。随即停用阿司匹林及氯吡格雷,静脉滴注甲泼尼龙琥珀酸钠40 mg,输注1个治疗单位的血小板(2.5×10¹¹个血小板,250mL,去白细胞辐照单采血小板),同时予泮托拉唑40 mg,每日2次静脉滴注。治疗3小时后复查血小板计数为 5×10⁹/L,此后 5 天内血小板计数逐步恢复正常。当血小板计数回升至 84×10⁹/L 以上时,重启阿司匹林及氯吡格雷治疗。治疗期间,患者未出现出血症状,最终顺利出院。出院后门诊规律随访 1 年,血小板计数持续稳定。患者血小板计数变化趋势见图1。
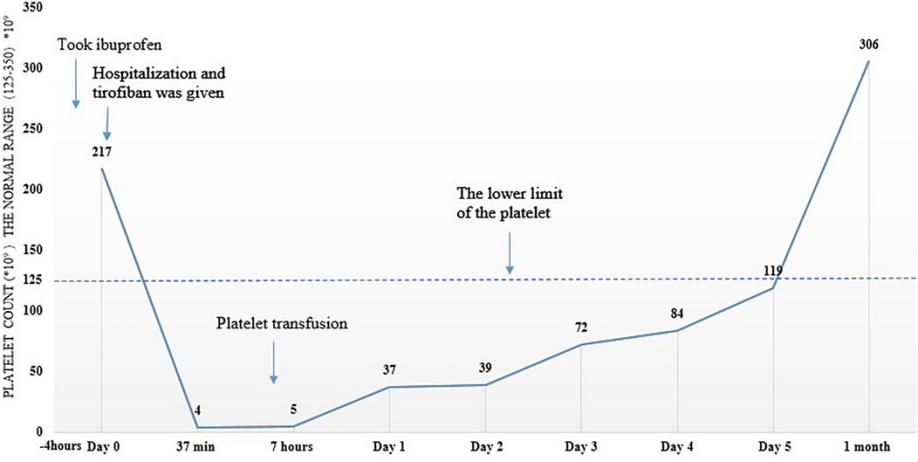
图 1 病例1患者血小板计数随时间变化趋势线图。患者入院前服用布洛芬,入院时血小板计数正常;替罗非班静脉输注后极短时间内,血小板计数急剧下降,由 217×10⁹/L 降至 4×10⁹/L;输注血小板 7 小时后,计数升至 5×10⁹/L;随后呈逐步上升趋势,第 5 天恢复至 119×10⁹/L,1 个月后升至 306×10⁹/L。图中虚线标注血小板正常参考范围
病例2
患者2为 44 岁女性,既往有高血压、高脂血症病史3年,因脑动脉支架植入术后复查收入本院神经内科。患者6个月前因反复发作性右侧肢体无力入院,经检查诊断为右侧颈内动脉 C7段重度狭窄,并行支架植入术。术后即刻予替罗非班以0.15μg/kg/min 的速率静脉输注,维持输注14小时,治疗期间未出现血小板计数下降。颅内支架植入术后,患者长期规律口服阿司匹林0.1 g/d、替格瑞洛90 mg / 次,每日2次抗血小板治疗。本次入院后,患者频繁出现左侧肢体麻木、无力发作,症状持续数分钟后可自行缓解。结合患者存在多发脑动脉狭窄闭塞、血管条件差、短暂性脑缺血发作(TIA)反复发作且病情进展风险高的临床特点,予替罗非班静脉输注治疗,先以0.1μg/kg/min 的速率输注30分钟,随后以0.05μg/kg/min 的速率维持输注。治疗后,患者左侧肢体麻木无力症状未再发作,替罗非班输注17小时后停药,复查血小板计数为219×10⁹/L,处于正常范围。为进一步明确血管病变情况,患者接受数字减影血管造影(DSA)检查,结果提示:颈内动脉支架内重度再狭窄,左侧大脑中动脉起始段闭塞,右侧大脑前动脉 A2 段闭塞,左侧大脑前动脉 A1 段重度狭窄。
DSA术后,患者主诉右侧腹股沟穿刺部位压痛。超声检查提示:右侧盆腔髂血管旁混合回声包块,考虑为血肿形成。复查血常规未见进行性出血表现。经血管外科会诊后,予患者口服布洛芬0.3g / 次,每日2次镇痛治疗。DSA术后第5天,患者突发右侧面部及肢体阵发性麻木。头颅计算机断层扫描(CT)检查排除颅内出血,遂再次予替罗非班以0.05μg/kg/min 的速率静脉输注。输注18小时后,血常规检查提示血小板计数降至6×10⁹/L。测患者腋温37.8℃,动脉血氧饱和度 99%,血压136/72 mmHg。立即停用替罗非班、布洛芬及所有抗血小板药物,皮下注射重组人血小板生成素(rhTPO,沈阳三生制药股份有限公司,商品名:特比澳)1 次,剂量为 300 U/kg。次日复查血小板计数升至44×10⁹/L,但患者继发大面积脑梗死,于2天后死亡。患者血小板计数变化趋势见图 2。
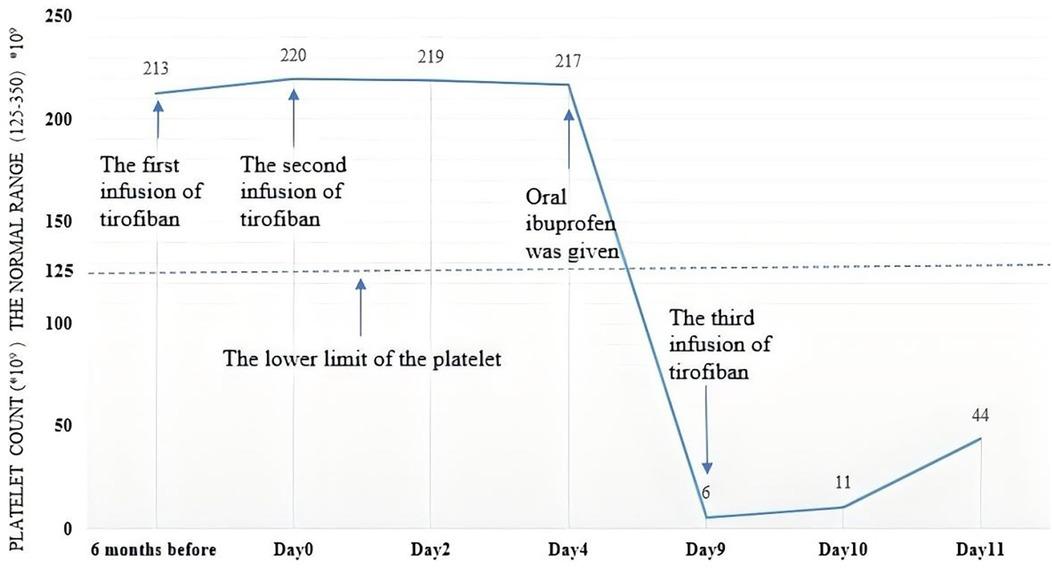
图 2 病例 2 患者血小板计数随时间变化趋势线图,图中标注关键时间节点的血小板计数
入院前 6 个月血小板计数为 213×10⁹/L;入院当日(第 0 天)为 220×10⁹/L;第 4 天口服布洛芬后为 217×10⁹/L;第 9 天第三次输注替罗非班后,血小板计数骤降至 6×10⁹/L;第 11 天回升至 44×10⁹/L。图中标注血小板正常参考范围为 125-350×10⁹/L。
血小板减少症可对患者临床预后产生不良影响,但临床医生往往难以精准识别血小板减少症的高危人群。多种药物可通过非免疫或免疫机制诱发血小板减少症。药物诱导性血小板减少症是一类临床诊断难度大、易被漏诊,且可能引发严重出血并发症的疾病。因此,早期识别高危人群并及时干预具有重要临床意义。本研究中2例患者既往均无血小板减少症病史,入院基线血常规检查血小板计数均正常,在排除原发性血小板减少症后,结合患者替罗非班与布洛芬联用的用药史,推测两种药物之间可能存在相互作用,进而诱发血小板减少症。
通过梳理患者1用药清单并查阅相关文献,认为替罗非班作为血小板糖蛋白(GP)Ⅱb/Ⅲa 受体拮抗剂,是诱发血小板减少症的潜在病因。替罗非班可竞争性结合血小板 GPⅡb/Ⅲa 受体,阻止纤维蛋白原黏附,从而促使超急性血栓溶解。
临床研究证实,替罗非班能够有效提高脑动脉再通率及脑组织灌注水平,缩小梗死灶体积,改善患者神经功能预后,对于错过静脉溶栓时间窗的急性缺血性脑卒中进展型(AIS-END)患者的预后改善具有积极作用。此外,多项研究表明,在脑血管疾病介入治疗中应用替罗非班,可显著提升患者临床疗效。因此,近年来替罗非班在心血管及脑血管疾病治疗中的应用日益广泛。尽管替罗非班诱发血小板减少症的病例已有报道,但引发极重度血小板减少症的情况仍十分罕见 。临床研究数据显示,替罗非班相关重度血小板减少症的发生率仅为 0.1%-0.5%,血小板计数低于 20×10⁹/L 的情况尤为少见。本研究病例1的最低血小板计数仅为 4×10⁹/L,停用替罗非班后,患者血小板计数逐步恢复正常。目前,替罗非班诱发血小板减少症的具体机制尚未明确,可能的机制为:替罗非班与血小板 GPⅡb/Ⅲa 受体结合后,导致受体构象发生改变,形成新的抗原决定簇,增强与体内已存在的药物依赖性抗体的亲和力,促使抗体与新抗原决定簇结合,进而加速血小板的破坏与清除。
本研究中病例2的诊疗过程进一步为上述推测提供依据。该患者6个月前因脑血管支架植入术,曾接受14小时替罗非班静脉输注治疗,期间未出现血小板计数下降;本次入院后,首次接受17小时替罗非班静脉输注,血小板计数仍维持正常水平。而当患者因疼痛口服布洛芬后,再次输注替罗非班,随即发生血小板减少症。唯一的变量在于本次治疗中,患者在输注替罗非班的同时,口服了布洛芬镇痛。再次回顾病例 1 的诊疗细节,发现患者在入院前 4 小时也曾服用布洛芬缓解头痛。
文献报道血小板减少症是部分非甾体抗炎药的罕见不良反应,涉及药物包括双氯芬酸、萘普生及布洛芬等。布洛芬主要通过抑制环氧合酶(COX)发挥抗炎、镇痛及解热作用。环氧合酶存在两种同工酶,即 COX-1 和 COX-2。其中 COX-1 在血小板中持续表达,可促进血小板聚集。非甾体抗炎药干扰血小板功能的主要机制为:可逆性抑制血小板内 COX-1 的活性,减少前列环素(PGI₂)和血栓素 A₂(TXA₂)的合成,而这两种物质均在血管舒张和血小板聚集中发挥关键作用。
波士顿大学医学中心开展的一项关于甾体抗炎药罕见严重不良反应的队列研究显示,多例重度血小板减少症由甾体抗炎药诱发。Meyer等人曾报道1例 71 岁女性患者,既往无血液系统疾病史,因服用布洛芬诱发免疫性血小板减少症,入院时表现为广泛出血性紫癜、瘀点及鼻出血。Medford等人报道1例71岁非洲裔男性患者,因长期服用布洛芬,继发血小板减少症、自身免疫性溶血性贫血、急性肝衰竭及间质性肾炎。布洛芬可能通过其代谢产物诱发免疫性血小板减少症。加拿大一项关于药物诱导性血小板减少症实验室诊断的系统性评价指出,16 种药物符合 DITP 确诊的实验室诊断标准,布洛芬位列其中。布洛芬临床应用广泛,常用于缓解轻至中度疼痛、退热及改善痛经症状。自 2019 年新型冠状病毒肺炎疫情暴发以来,布洛芬也被推荐用于新冠病毒感染相关症状的对症治疗。
本研究中 2 例患者既往均多次服用布洛芬,且未出现血小板减少症。因此认为布洛芬并非导致患者发生极重度血小板减少症的单一诱因。结合2例病例的共性特征,推测替罗非班与布洛芬联用可能协同增加了重度血小板减少症的发生风险。但二者相互作用的具体机制仍有待阐明,本次临床观察结果也无法完全排除巧合的可能性。多项针对健康志愿者的实验室研究及临床研究均表明,抗血小板药物与其他常用药物之间存在不良相互作用。阿司匹林与非甾体抗炎药的结合位点均位于环氧合酶核心区域的狭窄疏水通道内,已有研究证实二者存在竞争性相互作用的可能性。布洛芬通过短暂阻断 COX-1 介导的血栓素 A₂合成,抑制血小板聚集,从而增加出血风险。此外,卡泰拉劳森等人的关键性研究证实,布洛芬可干扰阿司匹林对 COX-1 的不可逆抑制作用。
目前学界认为,布洛芬与阿司匹林的相互作用机制为:布洛芬可竞争性占据血小板环氧合酶的结合位点,阻碍阿司匹林与该酶的结合。尽管关于替罗非班与布洛芬联用诱发药物诱导性血小板减少症的文献报道较少,但我们推测,二者联用可能通过类似的协同作用机制,加重血小板减少程度,提升出血风险。随着临床治疗手段的不断丰富,多种药物联用已成为临床治疗的常态,这也导致药物相互作用的发生概率不可避免地升高,临床需对此保持高度警惕。
一旦确诊药物诱导性血小板减少症,需立即停用可疑药物,并根据患者是否合并出血并发症,调整其他抗栓药物的使用方案。若患者血小板计数低于 10×10⁹/L,且出血风险较高,可考虑输注血小板及使用血小板生成素治疗。但需注意,输注血小板联合血小板生成素治疗可能诱发支架内血栓、急性心肌梗死及脑梗死等严重并发症,本研究中病例2在接受血小板生成素治疗后即发生致死性大面积脑梗死。因此,临床决策时需审慎权衡治疗获益与潜在风险。对于输注血小板后血小板计数仍持续偏低、无回升趋势的患者,可考虑加用免疫球蛋白治疗 。临床使用具有 DITP 风险的药物时,建议在用药后 2-6 小时检测首次血小板计数,此后每日监测,以便及时发现绝大多数血小板减少症病例。同时,应尽量避免联用多种具有血小板减少风险的药物,防止病情加重。
本研究中 2 例病例的共性特征为:替罗非班与布洛芬联用后,患者血小板计数均出现急剧、重度下降。这提示临床在联用替罗非班与布洛芬时需格外谨慎。建议对于联用两种药物的患者,需密切监测血小板计数,并严密观察有无出血倾向。若患者存在镇痛需求,可优先考虑选用对乙酰氨基酚等替代药物。若临床确需联用,则必须在治疗初始 24 小时内,每 6-12 小时强化监测血小板计数。若两种药物均需使用,需高频次密切监测患者血小板计数,及时发现血小板计数的急剧下降,降低出血风险。
结论
DITP是一种罕见但潜在危险的副作用,可能危及生命。两例在联合使用替罗非班和布洛芬背景下发生的严重血小板减少症提示两者之间存在潜在的相互作用。建议在联合使用替罗非班和布洛芬的患者中监测血小板计数并观察出血倾向。
医博士编译自:Zhu J, Chen C, Zhu C, et al. Case Report: Severe thrombocytopenia in the context of concomitant tirofiban and ibuprofen use: does ibuprofen matter? Front Cardiovasc Med. 2025; 12:1672200. doi:10.3389/fcvm.2025.1672200.
声明: 所有注明“来源:医博士”的文字、图片和音视频资料,版权均属于医博士所有,转载须注明“来源:医博士”;所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。