信迪利单抗和西达本胺治疗难治性转化弥漫性大B细胞淋巴瘤
来源:医博士 | 2022-01-19 作者:李胜佳
粘膜相关淋巴组织(MALT)淋巴瘤是一种惰性淋巴瘤,通常预后良好且进展缓慢。MALT淋巴瘤患者的中位总生存期(OS)为12.6年。然而,MALT淋巴瘤的组织学转化(HT)可能导致更具侵袭性的表型,例如弥漫性大B细胞淋巴瘤(DLBCL),但惰性淋巴瘤的转化频率较低。与非转化型MALT淋巴瘤相比,DLBCL患者预后较差,5年OS从86%降低至65%。此外,DLBCL没有标准方案。
西达本胺是一种组蛋白去乙酰化酶抑制剂(HDACi),在中国获批用于治疗R/R外周T细胞淋巴瘤。最近的研究表明,西达本胺可以诱导DLBCL细胞系的细胞凋亡,增强免疫细胞介导的肿瘤细胞的细胞毒性,并显示出抗肿瘤活性。程序性细胞死亡蛋白1(PD-1)抗体是一种靶向PD-1免疫检查点的药物,已成为多种类型肿瘤的治疗方法。然而,PD-1抗体作为单药治疗R/R DLBCL的疗效并不理想。一项关于纳武单抗单药治疗R/R DLBCL的II期研究表明,在自体干细胞移植(ASCT)不合格和ASCT失败的队列中,总缓解率(ORR)分别为3%和10%。
最近,几项临床前研究表明,HDACi可以增强免疫细胞活性并增强对PD-1抗体的反应。HDACi和PD-1抗体的组合可以协同增强抗肿瘤活性。在此,本病案报道了一例同时应用信迪利单抗和西达本胺治疗R/R tDLBCL的病例。
病例介绍
2018年2月,一名71岁男性患者,既往无肺部疾病史,主诉左胸区隐痛;疼痛扩大到左侧腋窝。胸部计算机断层扫描(CT)显示双肺多发斑片状磨玻璃影,弥漫性高密度点状阴影,纵隔多发小淋巴结。根据右肺空心针活检病理分析,患者被诊断为MALT淋巴瘤。活检组织的免疫组织化学分析显示淋巴瘤细胞:CD3(-)、CD20(+)、Bcl-2(+)、CD23(-)、CD10(-)、Bcl-6(-)、CD5(-)、细胞周期蛋白D1(-)、Mum-1(-)和Ki-67(10%)。此外,正电子发射断层扫描/CT(PET/CT)扫描显示,双侧肺多发斑片状高密度阴影和右下叶内侧基底节段巨大阴影中的氟脱氧葡萄糖(FDG)摄取增加。考虑到缺乏明确的治疗指征,患者采取观察等待策略。
2020年6月,患者因右大腿后侧持续疼痛入院。疼痛逐渐扩大到右腿和足底,并伴有麻木感。患者无法站立,右下肢开始逐渐出现凹陷性水肿。体格检查显示患者有周围性面瘫,ECOG评分3分。PET/CT复查(图1A)显示多个斑片状阴影中FDG摄取增加,双侧肺、双侧肾上腺、多发性骨骼和腰骶神经根大量实变。通过针吸活检获得肾上腺肿块活检组织。根据病理分析,患者被诊断为DLBCL,一种非生发中心B细胞样(non-GCB)亚型。活检组织的免疫组织化学分析显示淋巴瘤细胞:CD20(+)、Bcl-2(+)、CD23(-)、CD10(-)、Bcl-6(+)、CD5(-)、细胞周期蛋白D1(-)、Ki-67(70%)、Mum-1(+)、c-Myc(<10%+)和SOX11(-)。荧光原位杂交试验EBERISH、MYC和BCL2/IGH阴性。腰椎穿刺检查发现脑脊液(CSF)压力(205mmH2O)、蛋白质浓度(0.9g/L,正常参考值:0.15–0.45g/L)和IL-10浓度(235.0ng/L,正常参考值:4.3–6.9ng/L)升高。脑脊液细胞学检查可见一些非典型细胞。此外,CSF的流式细胞术检查显示κ限制性异常B细胞占核细胞的13.1%,表明中枢神经系统受累。通过下一代测序(Illumina)检测循环DLBCL游离DNA检测到以下突变:BCL6(2.8%)、TNFRSF(1.36%)、CREBBP(0.9%)、PIM1(0.8%)、MEF2B(0.6%)、BCL2(0.6%)和MALT1-BIRC3融合(0.3%)。肝肾功能检查和血常规检查结果基本正常,乳酸脱氢酶浓度正常。根据既往MALT淋巴瘤病史,患者被诊断为转化型DLBCL(Ann Arbor IVB分期和国际预后指数为4),具有广泛的淋巴结外受累和中枢神经系统受累。
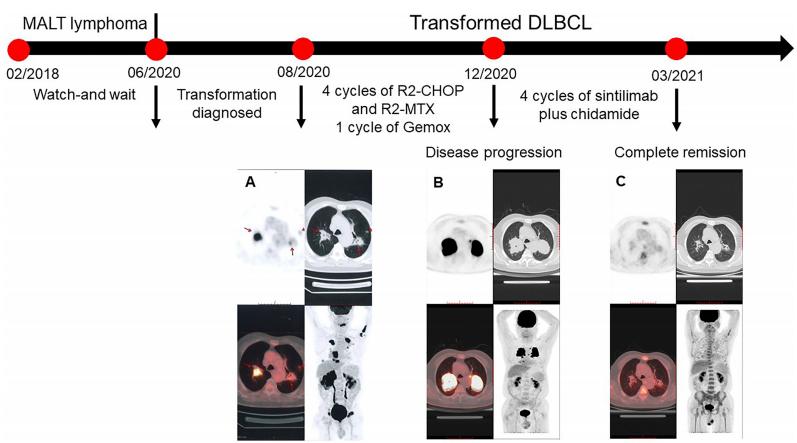
图1. 患者的PET/CT扫描。
2020年8月20日,患者因全身和中枢神经系统病变,接受了4个周期的R2-CHOP(利妥昔单抗、来那度胺、环磷酰胺、表柔比星、长春新碱、泼尼松)和R2-大剂量MTX(利妥昔单抗、来那度胺、和甲氨蝶呤)替代方案作为一线治疗。在每个周期中,患者还接受了甲氨蝶呤(10mg)、地塞米松(5mg)和阿糖胞苷(50mg)的鞘内注射。然而,在四个周期的治疗后,中期PET/CT扫描(图1B)显示肺和纵隔病变和FDG摄取增加(SUVmax=31.5),其他病变的大小显著减小。腰椎穿刺复检显示脑脊液压力(180mmH2O)和蛋白质浓度(0.66g/L)降低。根据中期检查,肺部和纵隔病变显示疾病进展,尽管中枢神经系统和其他外周受累处于缓解期。肺活检证实存在淋巴瘤。2020年12月20日,治疗转为一个周期的Gemox方案(吉西他滨和奥沙利铂)作为二线治疗,仍提示疾病进展。对于原发性难治性tDLBCL,没有首选方案。重复病理分析活检显示淋巴瘤仍为DLBCL,PD-L1表达。图2)。该患者还具有CREBBP突变。既往研究表明,PD-L1表达与PD-1抗体敏感性相关,乙酰转移酶CREBBP的突变表明HDACi可能有效。因此,患者接受信迪利单抗加西达本胺作为补救治疗。信迪利单抗的剂量为每周期静脉注射200mg,西达本胺的剂量为每周2次口服30mg,每21天重复一个疗程。四个周期的联合治疗后,PET/CT扫描(图1C)表明,根据2014年卢加诺标准,该患者被认为处于完全代谢缓解状态。腰椎穿刺证实了淋巴瘤的持续清除。
在联合治疗期间,患者经历了可控的不良事件。在第三个疗程中,患者出现血小板减少症(50×109/L),将西达本胺的剂量调整为每周2次口服20mg。在第四个周期中,他还出现了2级中性粒细胞减少症(1.18×109/L),这也被认为是由于西达本胺所致。治疗期间未发生胃肠道症状、皮疹、不适、肝肾损害等非血液学不良反应,未发生贫血或免疫相关不良反应。在撰写本文时,患者处于信迪利单抗和西达本胺联合治疗的第9个周期,没有任何症状或疾病进展的证据。
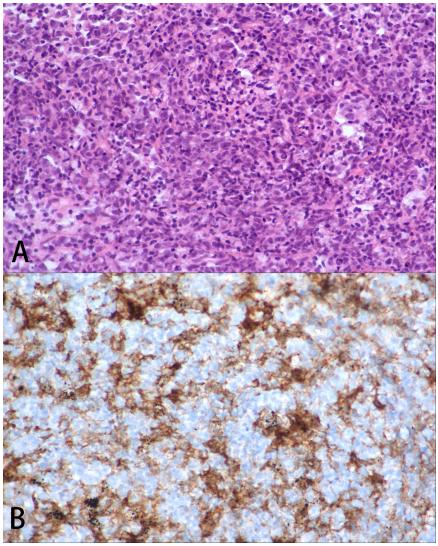
图2. 病理分析结果。
结论
本病例报告表明,信迪利单抗联合西达本胺可用于治疗R/R tDLBCL患者,但需要前瞻性临床试验来证明信迪利单抗联合西达本胺在R/R tDLBCL治疗中的显著疗效和良好的安全性。
医博士编译自:Chen C, Zhang W, Zhou D, et al. Sintilimab and Chidamide for Refractory Transformed Diffuse Large B Cell Lymphoma: A Case Report and A Literature Review. Frontiers in Oncology. 2021; 11:757403. doi:10.3389/fonc.2021.757403.
来源:https://pubmed.ncbi.nlm.nih.gov/34820328/
声明: 所有注明“来源:医博士”的文字、图片和音视频资料,版权均属于医博士所有,转载须注明“来源:医博士”;所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。